Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(\dfrac{x}{158}.........\dfrac{x}{158}........\dfrac{x}{158}\)
\(2Cu+O_2\underrightarrow{t^0}2CuO\)
\(\dfrac{y}{64}...........\dfrac{y}{64}\)
\(m_A=m_B\)
\(\Rightarrow x+y=\dfrac{x}{158}\cdot197+\dfrac{x}{158}\cdot87+\dfrac{80y}{64}\)
\(\Rightarrow x+y=\dfrac{142x}{79}+1.25y\)
\(\Rightarrow0.25y=-\dfrac{63}{79}x\)
\(\Rightarrow\dfrac{x}{y}=-\dfrac{79}{252}\)

Khối lượng oxi thoát ra: m O 2 = 197 + 3 – 152 = 48(g)
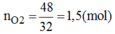
PTHH của phản ứng:
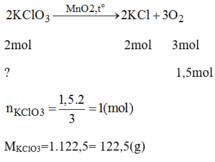
Khối lượng của KCl trong hỗn hợp ban đầu:
m K C l = 197-122,5 = 74,5(g)
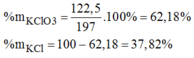

Gọi $n_{KMnO_4} = a(mol) ; n_{KClO_3} = b(mol) \Rightarrow 158a + 122,5b = 49,975(1)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$m_{O_2} = m_{giảm} = 4(gam)$
$\Rightarrow n_{O_2} = 0,5a + 1,5b = \dfrac{4}{32} = 0,125(2)$
Từ (1)(2) suy ra a = 0,339 ; b = -0,029 < 0
(Sai đề)

\(X:O_2\\ Y:KCl,CuO,Cu,KClO_4\left(có.thể.có\right)\\ Z:CO,CO_2,SO_2\\ KClO_3-^{^{ }t^{^{ }0}}->KCl+\dfrac{3}{2}O_2\\4 KClO_3-^{^{ }t^{^{ }0}}->KCl+3KClO_4\\ Cu+\dfrac{1}{2}O_2-^{^{ }t^{^{ }0}}->CuO\\ C+O_2-^{t^0}->CO_2\\ C_{dư}+\dfrac{1}{2}O_2-^{t^0}->CO\\ S+O_2-^{t^0}->SO_2\)

\(KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ 2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\\ m_{giảm}=\dfrac{1}{4}m_A\\ Đặt:x=n_{KMnO_4};y=n_{KClO_3}\left(x,y>0\right)\\ m_{O_2}=m_{giảm}=\dfrac{1}{4}m_A=\dfrac{1}{4}.\left(158x+122,5y\right)\\ Mặt.khác:m_{O_2}=32x+\dfrac{245}{3}y\\ \Rightarrow\dfrac{158x+122,5y}{4}=\dfrac{96x+245y}{3}\\ \Leftrightarrow90x=612,5y\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{612,5}{90}=\dfrac{245}{36}\\ \Rightarrow\%m_{\dfrac{KClO_3}{hhA}}=\dfrac{36.122,5}{36.122,5+245.158}.100\approx10,227\%\)

Do khối lượng chất rắn trong X và Y bằng nhau
=> Lượng O2 sinh ra khi phân hủy KClO3 phản ứng hết với Cu
PTHH: 2KClO3 --to--> 2KCl + 3O2
a--------------->1,5a
2Cu + O2 --to--> 2CuO
3a<--1,5a
=> b \(\ge\) 3a