Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

5.
\(n_X=\dfrac{2,24}{22,4}=0,1mol\\ M_X=2,125.4=8,5g\cdot mol^{^{ }-1}\\ n_{H_2}=a;n_{C_2H_4}=b\\ a+b=0,1\\ 2a+28b=8,5.0,1=0,85\\ a=0,075;b=0,025\\ H_2+C_2H_4-^{^{ }Ni,t^{^{ }0}}->C_2H_6\\ V_{C_2H_6}=0,025.22,4=0,56L;V_{H_2dư}=22,4\left(0,075-0,025\right)=1,12L\)
6.
Thu được Y chỉ gồm hydrocarbon nên khí hydrogen phản ứng hết.
\(n_A=\dfrac{4,48}{22,4}=0,2mol\\ n_Y=\dfrac{3,36}{22,4}=0,15mol\\ \Delta n_{hh}=n_{H_2\left(pư\right)}=0,05\left(mol\right)\\ n_{C_2H_4}=0,15\left(mol\right)\\ a.\%V_{H_2}=\dfrac{0,05}{0,2}=25\%\\ \%V_{C_2H_4}=75\%\\ b.BTLK\pi:0,15=0,05+n_{Br_2}\\ n_{Br_2}=0,1mol\)

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%
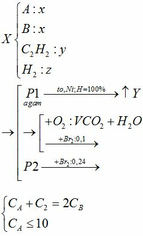
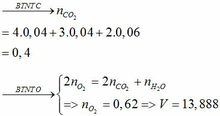



Ta có: \(n_Y=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow M_Y=\dfrac{1,32}{0,1}=13,2\left(g/mol\right)\)
→ Y gồm H2 dư và C2H6.
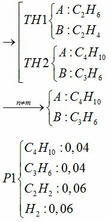
\(\Rightarrow\left\{{}\begin{matrix}n_{H_2\left(dư\right)}+n_{C_2H_6}=0,1\\2n_{H_2\left(dư\right)}+30n_{C_2H_6}=1,32\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{H_2\left(dư\right)}=0,06\left(mol\right)\\n_{C_2H_6}=0,04\left(mol\right)\end{matrix}\right.\)
Gọi: \(\left\{{}\begin{matrix}n_{H_2}=x\left(mol\right)\\n_{C_2H_2}=n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\)
BTNT C: 2y = 0,04 ⇒ y = 0,02 (mol)
Có: nH2 (pư) = 2nC2H2 + nC2H4 = 0,06 (mol)
⇒ nH2 = 0,06 + 0,06 = 0,12 (mol)
\(\Rightarrow V=\left(0,12+0,02+0,02\right).22,4=3,584\left(l\right)\)