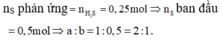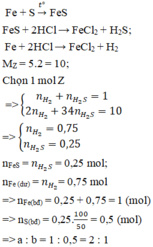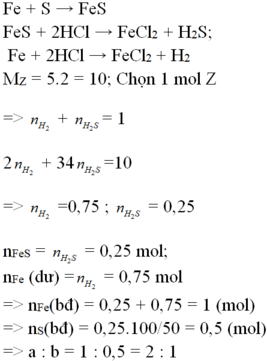Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng. Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
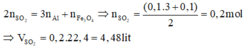

Đáp án B
Vì Al, Fe2O3, Fe3O4 có cùng số mol nên
![]()
Ý nung hỗn hợp trong điều kiện không có không khí chỉ dùng để đánh lạc hướng.Bài này ta chỉ cần sử dụng phương pháp bảo toàn electron.
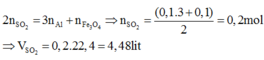

\(m_{dd\left(Br2\right)}=10,8\left(g\right)\) tăng là do C2H4 và C2H2 pứ
Hỗn hợp khí thoát ra gồm C2H6 và H2 do ko td với dd Br2
\(M=8.2=16\)
\(m=16.0,2=3,2\left(g\right)\)
Ap dụng đl bảo toàn khối lượng ta đc: mHH=m tăng+mkhí
\(\Leftrightarrow m_{hh}=10,8+3,2\Rightarrow m_{hh}=14\left(g\right)\)
Do số mol C2H2=nH2 nên ta gọi x là số mol của 2 chất
Ta có: \(26x+2x=14\left(M_{C2H2}=26;M_{H2}=2\right)\)
\(\Rightarrow x=0,5\left(mol\right)\)
\(n_{C2H2}=n_{H2}=0,5\left(mol\right)\)
\(PTHH:C_2H_2+\frac{5}{2}O_2\rightarrow2CO_2+H_2O\)
_______0,5________1,25__________
\(2H_2+O_2\rightarrow2H_2O\)
0,5___0,25____________
\(n_{O2\left(tong.o.2.PT.tren\right)}=1,25+0,25=1,5\left(mol\right)\)
\(\Rightarrow V_{O2}=1,5.22,4=33,6\left(l\right)\)

Đáp án C
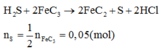
Chú ý: Không tồn tại muối sunfua của Al và Fe(III). H2S không phản ứng với AlCl3 nhưng nếu
![]()
Có sự khác nhau này do Fe3+ có tính oxi hóa mạnh còn Al3+ tính oxi hóa yếu

Đáp án A
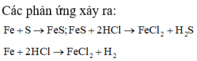
Hỗn hợp khí Z gồm H2S và H2. Đặt nFe=1mol . Dựa vào phương trình phản ứng ta thấy vì số mol khí sinh ra luôn là 1 mol với bất kì hiệu suất và tỉ lệ a:b nào nên:
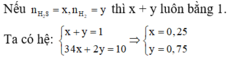
Theo đề bài hiệu suất phản ứng là 50% nhưng do chưa biết Fe hay S dư nên phải xét hai trường hợp. Tuy nhiên khi nhìn vào đáp án có thể thấy số mol sắt lớn hơn số mol lưu huỳnh nên hiệu suất được tính theo lưu huỳnh. Bảo toàn lưu huỳnh suy ra