Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

X gồm: CH4 và C2H4
C2H4 + Br2 => C2H4Br2
mC2H4Br2 = m/M = 37.6/188 = 0.2 (mol)
Theo phương trình ==> nC2H4 = 0.2 (mol)
CH4 + 2O2 => CO2 + 2H2O (1)
C2H4 + 3O2 => 2CO2 + 2H2O (2)
nC2H4 = 0.2 (mol) => nCO2(2) = 0.6 (mol)
VCO2 = 16.8 (l) => nCO2 = 16.8/22.4 = 0.75 (mol)
==> nCO2 (1) = 0.75 - 0.6 = 0.15 (mol)
==> nCH4 = 0.075 (mol)
Ta có: nCH4 = 0.075 (mol), nC2H4 = 0.2 (mol)
===> nhh = 0.275 (mol)
%nCH4 = 27.27%, %nC2H4 = 72.73%

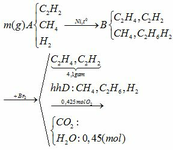
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)

a, Ta có \(n_{CH_4}+n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,05\left(mol\right)\\n_{C_2H_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{CH_4}=0,05.22,4=1,12\left(l\right)\\V_{C_2H_4}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
b, \(m_{CH_4}=0,05.16=0,8\left(g\right)\)
c, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,1\left(mol\right)\Rightarrow V_{ddBr_2}=\dfrac{0,1}{1}=0,1\left(l\right)\)
\(m_{C_2H_4}=0,1.28=2,8\left(g\right)\)

a)
Khí còn lại là CH4
\(n_{CH_4}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
=> \(n_{C_2H_4}=\dfrac{1,16-0,02.16}{28}=0,03\left(mol\right)\)
\(\%V_{CH_4}=\dfrac{0,02}{0,02+0,03}.100\%=40\%\)
\(\%V_{C_2H_4}=\dfrac{0,03}{0,02+0,03}.100\%=60\%\)
b)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,02-------------->0,02
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,03------------->0,06
=> nCO2 = 0,02 + 0,06 = 0,08 (mol)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,08----->0,08
=> mCaCO3 = 0,08.100 = 8 (g)

a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Giả sử: \(\left\{{}\begin{matrix}n_{C_2H_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{1,344}{22,4}=0,06\left(1\right)\)
Ta có: \(n_{Br_2}=\dfrac{16}{160}=0,1\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=x+2y\left(mol\right)\)
⇒ x + 2y = 0,1 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,02\left(mol\right)\\y=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,02}{0,06}.100\%\approx33,33\%\\\%\text{ }V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Ta có: 1/2 hỗn hợp khí gồm: 0,01 mol C2H4 và 0,02 mol C2H2.
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Theo PT: \(n_{CO_2}=2n_{C_2H_4}+2n_{C_2H_2}=0,06\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,06\left(mol\right)\)
\(\Rightarrow m_{cr}=m_{CaCO_3}=0,06.100=6\left(g\right)\)
Bạn tham khảo nhé!
X gồm: CH4 và C2H4
C2H4 + Br2 => C2H4Br2
mC2H4Br2 = m/M = 37.6/188 = 0.2 (mol)
Theo phương trình ==> nC2H4 = 0.2 (mol)
CH4 + 2O2 => CO2 + 2H2O (1)
C2H4 + 3O2 => 2CO2 + 2H2O (2)
nC2H4 = 0.2 (mol) => nCO2(2) = 0.6 (mol)
VCO2 = 16.8 (l) => nCO2 = 16.8/22.4 = 0.75 (mol)
==> nCO2 (1) = 0.75 - 0.6 = 0.15 (mol)
==> nCH4 = 0.075 (mol)
Ta có: nCH4 = 0.075 (mol), nC2H4 = 0.2 (mol)
===> nhh = 0.275 (mol)
%nCH4 = 27.27%, %nC2H4 = 72.73%
C2H4 + Br2 --> C2H4Br2
nC2H4Br2= 37.6/188=0.2 (mol)
=> nC2H4= 0.2 (mol)
nO2= 16.8/22.4=0.75 (mol)
C2H4 + 5/2O2 -to-> 2CO2 + 2H2O (2)
Từ PTHH (2):
=> nO2(2)= 0.2 *5/2= 0.5 (mol)
CH4 + 2O2 -to-> CO2 + 2H2O (3)
nO2 (3)= 0.75 - 0.5= 0.25 (mol)
Từ PTHH (3):
=> nCH4= 0.25/2= 0.125 (mol)
nX= 0.2 + 0.125= 0.325 (mol)
%CH4= 0.125/0.325 * 100%= 38.46%
%C2H4= 100 - 38.46= 61.54%