Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
nT = 0,02 mol
nCO2 = 0,04 mol
=> C = 0,04/0,02 = 2
Mà khi cho T vào dung dịch brom không có khí thoát ra nên X và Y chỉ có thể là C2H4 (x mol) và C2H2 (y mol)
{x+y=nT=0,02x+2y=nBr2=0,03→{x=0,01y=0,01{x+y=nT=0,02x+2y=nBr2=0,03→{x=0,01y=0,01
0,02 mol T chứa 0,01 mol C2H2
0,3 mol T chứa 0,15 mol C2H2
=> mAg2C2=0,15.240 = 36 gam

Đáp án C
nT = 0,02 mol
nCO2 = 0,04 mol
=> C = 0,04/0,02 = 2
Mà khi cho T vào dung dịch brom không có khí thoát ra nên X và Y chỉ có thể là C2H4 (x mol) và C2H2 (y mol)
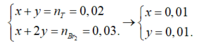
0,02 mol T chứa 0,01 mol C2H2
0,3 mol T chứa 0,15 mol C2H2
=> mAg2C2=0,15.240 = 36 gam

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron
Đáp án C
nT = 0,02 mol
nCO2 = 0,04 mol
=> C = 0,04/0,02 = 2
Mà khi cho T vào dung dịch brom không có khí thoát ra nên X và Y chỉ có thể là C2H4 (x mol) và C2H2 (y mol)
{x+y=nT=0,02x+2y=nBr2=0,03→{x=0,01y=0,01{x+y=nT=0,02x+2y=nBr2=0,03→{x=0,01y=0,01
0,02 mol T chứa 0,01 mol C2H2
0,3 mol T chứa 0,15 mol C2H2
=> mAg2C2=0,15.240 = 36 gam