Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

* Thí nghiệm 1: Cho hỗn hợp X tác dụng với dung dịch Br2
Đặt số mol anken A và ankin B lần lượt là x và y (mol)
nX = x + y = 0,5 (1)
CnH2n + Br2 → CnH2nBr2
x x
CmH2m-2 + 2Br2 → CmH2m-2Br4
y 2y
=> nBr2 = x + 2y = 0,8 (2)
Từ (1) và (2) ta có:
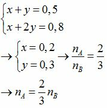
* Thí nghiệm 2: Đốt cháy hỗn hợp X
Hấp thụ CO2 vào dung dịch Ca(OH)2 thấy xuất hiện kết tủa, thêm KOH dư vào dung dịch thu được lại tiếp tục xuất hiện kết tủa nên ta có các phương trình hóa học sau:
CO2 + Ca(OH)2 → CaCO3 + H2O
0,25 ← 0,25
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 ← 0,025
Ca(HCO3)2 + 2KOH → K2CO3 + CaCO3 + 2H2O
0,025 ← 0,025
nCO2 = 0,25 + 0,05 = 0,3 mol
Ta có: m dung dịch giảm = mCaCO3 – mCO2 – mH2O => 7,48 = 25 – 0,3.44 – mH2O
=> mH2O = 4,32 gam => nH2O = 4,32/18 = 0,24 mol
Mặt khác, nB = nCO2 – nH2O = 0,3 – 0,24 = 0,06 mol
=> nA = 0,06(2/3) = 0,04 mol
BTNT C: nCO2 = n.nA + m.nB => 0,04n + 0,06m = 0,3
=> 2n + 3m = 15 (n≥2, m≥2)
| m |
2 |
3 |
4 |
| n |
4,5 |
3 |
1,5 |
Vậy A là C3H6 và B là C3H4
Khối lượng của hỗn hợp là: m = mC3H6 + mC3H4 = 0,04.42 + 0,06.40 = 4,08 (gam)

nhh khí = 7,84/22,4 = 0,35 (mol)
Gọi nCH4 = a (mol); nC2H6 = b (mol)
a + b = 0,35 (1)
nCaCO3 = 50/100 = 0,5 (mol)
PTHH:
CO2 + Ca(OH)2 -> CaCO3 + H2O
0,5 <--- 0,5 <--- 0,5
CH4 + 2O2 -> (t°) CO2 + 2H2O
a ---> 2a ---> a
2C2H6 + 7O2 -> (t°) 4CO2 + 6H2O
b ---> 3,5b ---> 2b
=> a + 2b = 0,5 (2)
Từ (1)(2) => a = 0,2 (mol); b = 0,15 (mol)
mCH4 = 0,2 . 16 = 3,2 (g)
mC2H6 = 0,15 . 30 = 4,5 (g)
%mCH4 = 3,2/(3,2 + 4,5) = 41,55%
%mC2H6 = 100% - 41,55% = 58,45%

Ptpư CnH2n+2 + Cl2 CnH2n+1Cl + HCl
CnH2n+2 + 2Cl2 CnH2nCl2 + 2HCl
HCl + NaOH → NaCl + H2O
Số mol NaOH = mol HCl = mol Cl2 = 0,3 mol
Theo ĐLBTKL: mankan = 15,75 + 36,5.0,3 – 71,0,3 = 5,4 gam
→ 0,15 < molankan < 0,3
→ 5,4/0,3 < Mankan < 5,4/0,15
→ 18 < 14n + 2 < 36
→ 1,14 < n < 2,43 → n = 2 → CTPT ankan: C2H6
hình như là ankan thì phải mik k rỏ về bài này lắm

Fe3O4+4CO=>3Fe+ 4CO2
CuO+CO=>Cu+CO2
Cr B gồm Fe Cu
HH khí D gồm CO dư và CO2
CO2 +Ca(OH)2=>CaCO3+H2O
p/100 mol<= p/100 mol
2CO2+Ca(OH)2 => Ca(HCO3)2
p/50 mol
Ca(HCO3)2+ 2NaOH=>CaCO3+ Na2CO3+2H2O
p/100 mol p/100 mol
Tổng nCO2=0,03p mol=nCO
=>BT klg
=>m+mCO=mCO2+mB=>mB=m+0,84p-1,32p=m-0,48p
c) hh B Fe+Cu
TH1: Fe hết Cu chưa pứ cr E gồm Ag Cu
dd Z gồm Fe(NO3)2
Fe+2Ag+ =>Fe2+ +2Ag
TH2:Cu pứ 1p cr E gồm Cu và Ag
Fe+2Ag+ => Fe2+ +2Ag
Cu+2Ag+ =>Cu2+ +2Ag
Dd Z gồm 2 muối của Fe2+ và Cu2+

CH3OH + 3/2O2 → CO2 + 2H2O (1) 0,2 mol 0,2mol 0,4mol
C2H5OH + 3O2 → 2CO2 + 3H2O (2)
0,1 mol 0,2mol 0,3mol
Theo pht phản ứng (1) và (2): nCO2 = 0,4 mol; nH2O = 0,7mol
nNaOH = 0,5 mol(mol)
1 < nNaOH : nCO2 = 0,5 : 0,4 = 1,25 < 2 → tạo ra 2 muối.
Gọi số mol của CO2 ở (3), (4) lần lượt là a và b.
2NaOH + CO2 → Na2CO3 + H2O (3)
2a a a
NaOH + CO2 → NaHCO3 (4)
b b b
Giải hệ phương trình: 2a+b=0,5; a+b=0,4
→ a = 0,1. b = 0,3.
mNa2CO3 = 106 x 0,1 = 10,6g. mNaHCO3 = 84 x 0,3 = 25,2gam.
Khối lượng dung dịch sau phản ứng: mdd = 100 + 44 x 0,4 + 18 x 0,7 = 130,2g
C% Na2CO3 = 8,14 %
C% NaHCO3 = 19.35 %

n X = 4,48/22,4 = 0,2 mol
=> n CH 4 = 0,2/4 = 0,05 mol; n A = 0,05 x 3 = 0,15 mol
Phương trình hóa học: CH 4 + 2 O 2 → C O 2 + 2 H 2 O
C n H m + (n+m/4) O 2 → t ° nC O 2 + m/2 H 2 O
C H 2 + Ca OH 2 → CaC O 3 + H 2 O
n CO 2 = n CaCO 3 = 50/100 = 0,5 mol => n CO 2 , n H 2 O tạo ra khi đốt cháy A là
n CO 2 = 0,5 - 0,05 = 0,45mol; n H 2 O = 0,7 - 0,1 = 0,6 mol
=> Công thức của A là C 3 H 8

Khi cho NaOH dư vào thu thêm được kết tủa nên dung dịch có muối Ca(HCO3)2.
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,5 ← 0,15
2CO2 + Ca(OH)2 → Ca(HCO3)2
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + 2H2O
0,1 ← 0,1
→ nCO2 = 0,1.2 + 0,5 = 0,7
Mặt khác: mdd giảm = mCaCO3 – mCO2 + mH2O
→ 9,12 = 50 – (44.0,7 + 18.nH2O) → nH2O = 0,56