Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có: Este đơn chức X + Este đa chức Y + NaOH → 2 muối + 2 ancol cùng số nguyên tử C
nNaOH= 0,56 mol , nCO2 = 0,72mol , nH2O =1,08mol
→ nancol = nH2O − nCO2= 0,36 mol
→ số C trong ancol = nCO2 nancol = n C O 2 n a n c o l = 0 , 72 0 , 36
→ Ancol là: C 2 H 5 O H : a m o l C 2 H 4 O H 2 : b m o l → n X : a m o l n Y : b m o l
Ta có hệ phương trình: a + b = 0 , 36 a + 2 b = 0 , 56 → a = 0 , 16 b = 0 , 2
Áp dụng định luật bảo toàn khối lượng ta có
m e s t e + m N a O H = m m u o i + m a n c o l → mmuoi= 43,12 (g)

Định hướng tư duy giải
Xử lý X
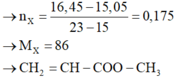
→Y là HCOO – CH2 – CH2 – OOCH →Z là HCOO – C3H6 – OOCH
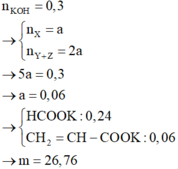

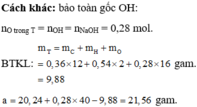


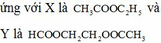

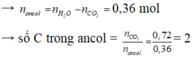
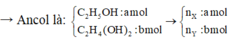
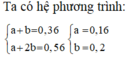
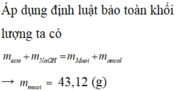
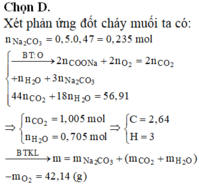

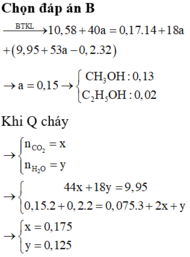

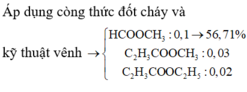





Đáp án B