Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt số mol NaCl: a (mol); NaBr: b (mol); NaI: c (mol)
a) Các phản ứng với brom dư:
2NaI + Br2 \(\rightarrow\) 2NaBr + I2
Hỗn hợp A: 58,5a + 103b + 150c = 5,76
Sau phản ứng với brom: 58,5a + 103 (b + c) = 5,29
\(\Rightarrow\) 47c = 0,47
* Các phản ứng với Cl2
2NaBr + Cl2 \(\rightarrow\) 2NaCl + Br2
2NaI + Cl2 \(\rightarrow\) 2NaCl + I2
Nếu Cl2 chỉ phản ứng với NaI thì khối lượng hỗn hợp muối sau phản ứng với
Cl2 là
5,76 - 1,5 + 0,585 = 4,845g.
Theo đề bài hỗn hợp sau phản ứng chỉ có 3,955 (g). Vậy Cl2 đã phản ứng với cả NaBr.
mhỗn hợp = 3,955 (g), trong đó có 0,05 (mol) NaCl và còn lại là NaBr.
nNaBr còn lại = \(\frac{3,955-0,05.58,5}{103}=0,01\left(mol\right)\)
Tính số mol NaBr tham gia phản ứng.
1 mol NaBr thay thế bằng 1 mol NaCl khối lượng giảm 44,5 g.
x mol NaBr thay thế bằng x mol NaCl khối lượng giảm 4,845 - 3,955 = 0,89 (g)
\(\Rightarrow\frac{0,89}{44,5}=0,02\)
Số mol NaBr có trong 5,76g = 0,02 + 0,01 = 0,03
\(n_{NaCL}=\frac{5,76-3,09-1,5}{58,5}=\frac{1,17}{58,6}=0,02\)
% theo khối lượng
NaCl: 20,3%; NaBr: 53,66%; NaI: 26,04%

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
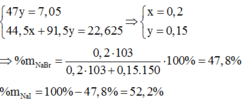

Đáp án B
Gọi x, y là số mol NaCl và NaI trong hh X
m(X) = m(NaCl) + m(NaI) = 58,5x + 150y = 104,25g (1)
Sục khí Cl2 dư vào dd A:
NaI + 1/2Cl2 → 1/2I2 + NaCl
y → y
mmuối = m(NaCl) = 58,5.(x+y) = 58,5g
→ x + y = 1mol (2)
Giải hệ PT (1), (2) ta được: x = 0,5mol và y = 0,5mol
mNaCl = 0.5.58,5 = 29,25 (g)

Gọi số mol của NaBr là x(mol) ,số mol của NaI là b(mol)
TH1 :\(m_{giam}=\left(127-80\right)x=7,05\)
\(\Rightarrow x=0,05\)
TH2 : \(m_{giam}=\left(127-35,5\right)x+\left(80-35,5\right).y=22,625\)
\(\Rightarrow y=0,2\)
\(\Rightarrow\%_{NaBr}=\frac{0,2.103.100}{0,2.102+0,15.150}=47,8\%\)

NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%

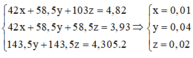
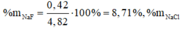
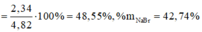
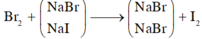
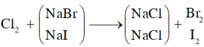
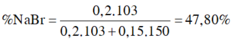
\(\left\{{}\begin{matrix}nNaCl=x\\nNaBr=y\\nNaI=z\end{matrix}\right.\)
ta có : \(58,5x+103y+150z=5,76\left(1\right)\)
TN1:
\(Br_2+2NaI\rightarrow2NaBr+I_2\)
z ----> z
\(\Rightarrow m_{muối}=mNaBr+mNaCl=103\left(y+z\right)+58,5x=5,29\left(2\right)\)
Từ (1) và (2) => z =0,01
TN2:
\(Cl_2+2NaI\rightarrow2NaCl+I_2\)
0,01 0,01
\(Cl_2+2NaBr\rightarrow2NaCl+I_2\)
\(nNaCl=nCl^-=0,05\rightarrow mNaCl=2,925\left(g\right)\)muối khan ngoài NaCl còn muối khác.Do \(I^-\) có tính khử mạnh hơn \(Br^-\) nên NaI sẽ hết trước và sau hai phản ứng NaBr còn dư.
\(nNaBr\left(dư\right)=t\)
\(\Rightarrow nNaCl=0,05=0,01+y-t+x\)
\(m_{muối}=mNacl+mNaBr\Rightarrow mNaBr_{\left(dư\right)}=3,955-0,05.58,5=1,03\)
\(\Rightarrow t=0,01\)
\(\Rightarrow x+y=0,05\left(3\right)\)
(1) ; (3) ; => \(x=0,02;y=0,03\)
\(\Rightarrow mNaCl=1,17\left(g\right)\)