Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\) ⇒ 24x + 56y = 16 (1)
Có: m dd tăng = mMg + mFe - mH2
⇒ mH2 = 16 - 15,2 = 0,8 (g) \(\Rightarrow n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\)
BT e, có: 2nMg + 2nFe = 2nH2 ⇒ x + y = 0,4 (2)
Từ (1) và (2) ⇒ x = y = 0,2 (mol)
BTNT H, có: nHCl = 2nH2 = 0,8 (mol)
\(\Rightarrow m_{ddHCl}=\dfrac{0,8.36,5}{20\%}=146\left(g\right)\)
⇒ m dd sau pư = 146 + 15,2 = 161,2 (g)
BTNT Mg, có: nMgCl2 = nMg = 0,2 (mol)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{0,2.95}{161,2}.100\%\approx11,79\%\)

Đáp án A
Gọi M là kim loại chung cho Zn và Mg với hóa trị n
Sơ đồ phản ứng: M + H 2 SO 4 ( loãng , dư ) → M 2 ( SO 4 ) n ⏟ muối + H 2 ↑
Khí thu được là
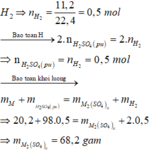

Đáp án D
Số mol H2 thu được là : n H 2 = 11 , 2 22 , 4 = 0 , 5 mol
Gọi M là kim loại chung cho Al và Mg với hóa trị n
Sơ dồ phản ứng :
M ⏟ 10 , 2 gam + H 2 S O 4 ( l o ã n g , d ư ) → M 2 ( S O 4 ) n ⏟ m u ố i + H 2 ↑ ⏟ 0 , 5 m o l
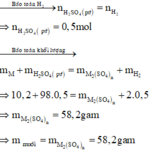

Đáp án D
Số mol H2SO4 là: n H 2 SO 4 = 0 , 5 . 0 , 1 = 0 , 05 mol
Gọi M2On là oxit chung cho các oxit trong X
Sơ đồ phản ứng :
![]()
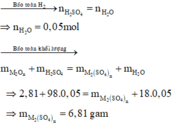

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
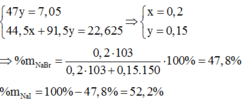

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)