Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%

Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.

B3:
Bài 3 người ta cho các kim loại sau đây là những kim loại nào thế?
B2:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\\ MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\\ Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+H_2O\\ Mg\left(OH\right)_2\rightarrow\left(t^o\right)MgO+H_2O\\ Đặt:n_{Al}=a\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}27a+24b=10\\40b=6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=\dfrac{32}{135}\\b=0,15\end{matrix}\right.\\ \Rightarrow\%m_{Mg}=\dfrac{0,15.24}{10}.100\%=36\%\)

Đáp án B
Đặt
![]()
Khối lượng muối khan giảm là do đã xảy ra phản ứng thay thế các nguyên tử halogen trong muối.
Ta có hệ:
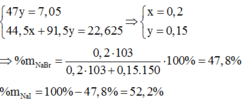

Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)
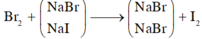
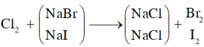
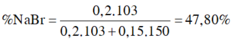

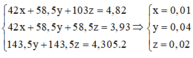
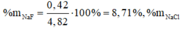
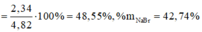
Đáp án C