

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


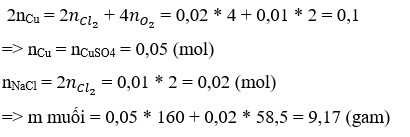

Chọn A.
Tại t = 4825 (s) Þ ne = 0,1 mol
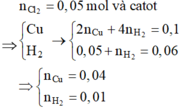
Tại t = 7720 (s) Þ ne = 0,16 mol Þ Tại anot Cl2 (x) và O2 (y) còn catot Cu (0,04) và H2 (z)
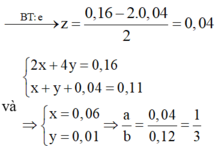

∑ne trao đổi = 0,3 mol < 2nCu2+.
⇒ Cu chưa bị điện phân hết và khí thoát ra là Cl2 và có thể có cả O2.
Nếu chỉ có khí Cl2
⇒ Quy đổi mDung dịch giảm = mCuCl2 = 0,15×135 = 20,25 ≠ 14,75 ⇒ Loại.
+ Vậy có cả O2 thoát ra
⇒ mDung dịch giảm = mCuCl2 + mCuO.
+ Đặt số mol 2 chất lần lượt là a và b ta có:
a + b = 0,15 mol (PT bảo toàn Cu).
135a + 80b = 14,75 (PT theo m dung dịch giảm).
+ Giải hệ ⇒ a = nCuCl2 = 0,05 mol
⇒ nNaCl = 0,05×2 = 0,1 mol.
⇒ CM NaCl = 0 , 1 0 , 2 = 0,5M
Đáp án D

Đáp án D
∑ne trao đổi = 0,3 mol < 2nCu2+.
⇒ Cu chưa bị điện phân hết và khí thoát ra là Cl2 và có thể có cả O2.
Nếu chỉ có khí Cl2 ⇒ Quy đổi mDung dịch giảm = mCuCl2 = 0,15×135 = 20,25 ≠ 14,75 ⇒ Loại.
+ Vậy có cả O2 thoát ra ⇒ mDung dịch giảm = mCuCl2 + mCuO.
+ Đặt số mol 2 chất lần lượt là a và b ta có:
a + b = 0,15 mol (PT bảo toàn Cu).
135a + 80b = 14,75 (PT theo m dung dịch giảm).
+ Giải hệ ⇒ a = nCuCl2 = 0,05 mol ⇒ nNaCl = 0,05×2 = 0,1 mol.
⇒ CM NaCl = 0,1/0,2 = 0,5M

Chọn đáp án B
Nhận thấy bên anot điện phân Cl- trước rồi đến H2O
Bên catot điện phân Cu2+ rồi đến H2O
Khối lượng dung dịch giảm gồm CuCl2: 0,125 mol và CuO
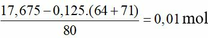
→
dung dịch Y chứa Cu2+ : 0,265 mol và H+ : 0,02 mol, SO42-, Na+
Khi thêm bột Fe xảy ra phản ứng: Fe + 2H+ → Fe2+ + H2 và Fe + Cu2+ → Fe2+ + Cu
Chất rắn thu được gồm Cu: 0,265 mol, Fe dư:
m= 18 - 56.(0,265 + 0,01) + 0,265.64 = 19,56 gam