Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1
a) M+2HCl--->MCL2+H2
Ta có
n H2=6,72/22.4=0,3(mol)
Theo pthh
n M=n H2=0,3(mol)
M=\(\frac{19,5}{0,3}=65\)
Vậy M là Zn(kẽm)
b) Theo pthh
Theo pthh
n ZnCl2=n H2=0,3(mol)
m ZnCl2=0,3.136=40,8(g)
Bài 2
a)2M+2nH2O--->2M(OH)n+nH2
Ta có
n H2=0,48/2=0,24(mol)
Theo pthh
n M=2/n n H2=0,48/n (mol)
M=3,33:0,48/n=7n
+n=1------->M=7(li)
b)Theo pthh
n Li=2n H2=0,48(mol)
CM LiOH=0,48/0,1=4,8(M)
Bài 3
M+2HCl---->MCl2+H2
Ta có
n H2=0,672/22,4=0,03(mol)
Theo pthh
n M=n H2=0,03(mol)
M=0,72/0,03=24
Vậy M là magie..kí hiệu Mg

Đặt 2 kim loại hóa trị II là A và B (giả sử MA < MB)
PTHH: A + 2HCl\(\rightarrow\) ACl2 + H2 (1)
B + 2HCl \(\rightarrow\) BCl2 + H2 (2)
nHCl = VHCl. CM = 0,5. 1 = 0,5 (mol)
TH1: hh kim loại và HCl pư hết, dd thu được sau pư chứa ACl2 và BCl2
Theo PTHH (1) và (2):
có nACl2 + nBCl2 = \(\frac{1}{2}\)nHCl = \(\frac{1}{2}\). 0,5 = 0,25 (mol)
Trong dd Y các chất tan có nồng độ mol bằng nhau => nACl2 = nBCl2
\(\Rightarrow\) nACl2 = nBCl2 = \(\frac{0,25}{2}\)= 0,125 (mol)
Theo PTHH (1): nA = nACl2 = 0,125 (mol)
Theo PTHH (2): nB = nBCl2 = 0,125 (mol)
Mà mhh = 4,9
\(\Rightarrow\)0,125.MA + 0,125.MB = 4,9
\(\Rightarrow\) MA + MB = 39,2 \(\rightarrow\) Loại vì MA + MB phải chẵn
TH2: hh kim loại pư hết, HCl còn dư sau pư
Theo bài: nồng độ mol/l các chất tan trong dd Y bằng nhau
\(\Rightarrow\) nHCl dư = nACl2 = nBCl2 = x (mol)
BTNL "Cl: có nHCl dư + 2nACl2 + 2nBCl2 = nHCl bđ
\(\Rightarrow\)x + 2x + 2x = 0,5
\(\Rightarrow\)5x = 0,5
\(\Rightarrow\)x = 0,1 (mol)
Theo (1): nA = nACl2 = 0,1 (mol)
Theo (2): nB = nBCl2 = 0,1 (mol)
\(\Rightarrow\)0,1.MA + 0,1. MB = 4,9
\(\Rightarrow\) MA + MB = 49
Kẻ bảng có MA = 9 và MB = 40 thỏa mãn
Vậy A là Be còn B là Ca
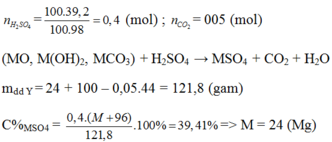

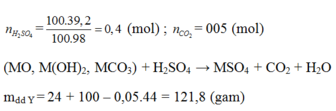





Chọn C