Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.

a/
PTHH:
FeO + CO => Fe + CO2 (1)
Fe2O3 +3CO => 2Fe + 3CO2 (2)
CuO + CO => Cu + CO2 (3)
CO2 + Ca(OH)2 => CaCO3 + 2H2O
b/
-m gam hh X{Fe,FeO,Fe2O3,CuO} + hh Y {CO,CO2} => 20 g A + Z (*)
nCO2 sau phản ứng = nCaCO3 = 0,4mol
Khí G thoát ra là CO dư
V(CO dư) = 0,2 V (Z) hay nCO dư= 0,2. (nCO2 sau phản ứng + nCO dư) => nCO dư=0,1 mol
=> mZ = 0,1.28 + 0,4.44=20,4 g
nY = nCO ban đầu + nCO2 ban đầu(trong hhY) = nCO pư + nCO dư + nCO2 ban đầu(trong hhY)
mà nCO pư=nCO2 (1) (2) (3)
=> nY= nCO2 sau pư + nCO dư = 0,4 + 0,1 = 0,5 mol=> V(Y)=11,2 l
=> mY=D.V=11,2.1,393=15,6016
Theo ĐLBTKL(*) : m= 20+ 20,4-15,6016= 24,7984
Mg+H2SO4=MgSO4+H2
2Al+3H2SO4=Al2(SO4)3+3H2
nH2=2,24/22,4=0,1 mol
gọi x,y lần lượt là số mol của Mg và Al
ta có hệ phương trình 24x+27y=1,95
x+3/2x=0,1
giải ra được x=0,025 mol,y=0,05 mol
m mg=0,025.24=0,6g
%mMg=0,6.100/1,95=30,76%
%mAl=100-30,76=69,24%
nMg=nMgSO4=nH2SO4=0,025 mol
mMgSO4=0,025.120=3 g
nAl2(SO4)3=0,05.3/2=0,075 mol
mAl2(SO4)3=0,075.342=25,65 g
nH2SO4=0,05.3/2=0,075 mol
mH2SO4=(0,025+0,075).98=9,8 g
mdung dịch H2So4=9,8.100/6,5=150,7 g
mdung dịch sau phản ứng =1,95+150,7-0,1.2=152,45g
------>C%MgSO4=3.100/152,45=1,96
C%Al2(SO4)3=25,65.100/152,45=16,8

CT chung A+2nH2SO4-->A2(SO4)n+nSO2+2nH2O
0.035/n 0.035 (mol)
A2(SO4)n-->A2On
0.035/n 0.035/n
mr=mA+(0.035/n)*n*16=2g
trắc nghiệm nSO42-=nSO2=0.035
BTĐT( chất rắn nên tự luận ko ghi được):nO2-=nSO42-=0.035
mr=mA+mO2-=2
A+2nH2SO4-->A2(SO4)n+nSO2+2nH2O
0.035/n 0.035 (mol)
A2(SO4)n-->A2On
0.035/n 0.035/n
mr=mA+(0.035/n)*n*16=2g
trắc nghiệm nSO42-=nSO2=0.035
BTĐT( chất rắn nên tự luận ko ghi được):nO2-=nSO42-=0.035
mr=mA+mO2-=2
#GG
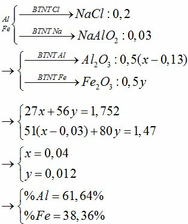
có n NO = 0,04 mol và dd có axit dư => ko tạo muối amoni
Al : x mol
Fe y mol
=> 27x + 56y = 1,95
3x +3y = 0,04.3
=> x =0,01 , y = 0,03
=> m Al = 0,27g, m Fe = 1,68 g
bạn gọi số mol của Fe(OH)2 : x mol
Fe(OH)3 : y mol
vì sau khi nung chỉ có Fe2O3 và Al2O3
0,015 0,0075
x + y = n Fe = 0,03 mol
n OH- = 4n Al 3+ - n kết tủa
=> 0,165 - 2x -3y = 4.0,03 - 0,015
=> 2x + 3y = 0,06
=> x = 0,03, y = 0 => Al đẩy Fe 3+ xuống Fe 2+ hoàn toàn
=> n Al tác dụng với HNO3 còn lại = 0,01 mol
=> n NO thoát ra = 0,01 mol
=> tổng n NO thoát ra = 0,05 mol
=> n HNO3 = 0,05.4 = 0,2 mol
=> Cm = 1,25 M