Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nhận thấy 9,2 gam oxit > 8,4 gam X → nên Ag+, Cu2+ phản ứng hết
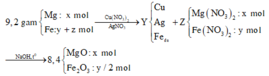
Gọi số mol Fe tham gia phản ứng là y mol, số mol Fe dư là x mol
→ nO2 pư để tạo thành Fe2O3 = y/4 mol
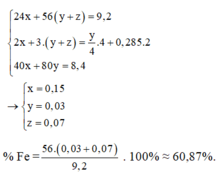
Đáp án A

Đáp án D
(Mg, Fe) + (AgNO3, Cu(NO3)2) => 3 kim loại
=> Chứng tỏ Mg, AgNO3, Cu(NO3)2 phản ứng hết, Fe còn dư; 3 kim loại là Ag, Cu, Fe.
Dung dịch Z chứa Mg(NO3)2 và Fe(NO3)2.
Đặt số mol Mg, Fe phản ứng, Fe dư lần lượt là a, b, c
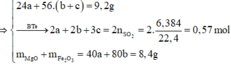
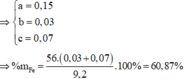

Đáp án B
B T K L : m O 2 = m K M n O 4 - m c r a n = 3 , 84 g ⇒ n O 2 = 0 , 12 m o l ⇒ n O = 0 , 24 m o l m M g , F e = m o x i t - m O = 13 , 04 - 0 , 24 . 16 = 9 , 2 g a m M g : x m o l F e : y m o l
⇒ % m M g = 39 , 13 %

Đáp án D:
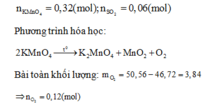
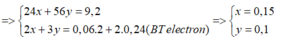
Gọi x và y lần lượt là số mol của Mg và Fe
=> 24x+56y = 9,2
Bảo toàn electron ta có
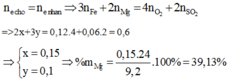
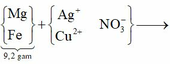
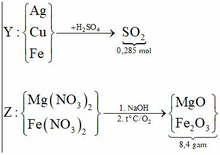


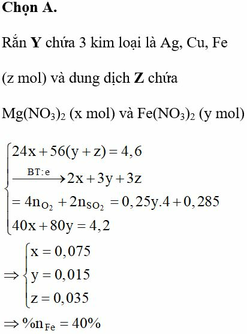
gọi x, y lần lượt là nFe, nCu
ta có 56x + 64y = 15,2 (1)
nSO2 = 6,72/22,4 = 0,3
Fe → Fe+3 + 3e S+6 + 2e → S+4
x → 3x 0,6 ← 0,3
Cu → Cu+2 + 2e
y → 2y
áp dụng định luật bảo toàn e ⇒ 3x + 2y = 0,6 (2)
từ (1) và (2)
x = 0,1
y = 0,15
% mFe = 0,1.56 / 15,2 = 36,84%
%mCu = 63,16%
b/ MNaHCO3 =84
MNa2CO3 = 106
giả sử 45,8 gam chất rắn tạo thành là muối
ta có nmuối = ns = nSO2 = 0,3
⇒Mmuối = 45,8/0,3 = 152,67 > MNa2co3 ⇒ trong 45,8 gam chất rắn có NaOH dư ⇒ tạo 1 muối Na2CO3 với nNa2CO3 = nS= nSO2= 0,3
mNa2co3= 0,3.106 = 31,8 ⇒ mNaOH dư = 45,8 - 31,8 = 14
\(\sum\)nNaOH = 2nNa2CO3 + 14/40 = 0,95
⇒V = 0,95/2 = 0,475 l
c. áp dụng định luật bảo toàn e
2H+1 + 2e → H2
2nH2 = 3nFe + 2nCu = 2nSO2 = 0,6
⇒ nH2 = 0,3 ⇒ V= 0,3.22,4 = 6,72l