Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C
Ta có nFe = 0,12 mol; nHNO3 = 0,4 mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
0,1 ← 0,4 → 0,1
(dư 0,02)
Fe còn dư + 2Fe(NO3)3 → 3Fe(NO3)2
0,02 → 0,04
(còn dư 0,06)
Dung dịch X chứa Fe(NO3)2 và Fe(NO3)3 còn dư
Khi cho Cu và dung dịch X thì:
Cu + 2Fe(NO3)3còn dư →Cu(NO3)2 + 2Fe(NO3)2
0,03 ← 0,06
Vậy mCu tối đa = 64.0,03 = 1,92g

Đáp án B
n N O = 0 , 15
Cho BaCl2 dư vào X thu được kết tủa là BaSO4 → n B a S O 4 = 0 , 05 m o l
Quy đổi hỗn hợp về Fe x mol, Cu y mol và S 0,05 mol (bảo toàn S).
=> 56x+64y+0,05.32= 5,2
Bảo toàn e: 2x+0,06+2y+0,05.6= 0,15.3 Giải ra nghiệm âm loại.
TH1: HNO3 hết thì X hòa tan được 0,03 mol Cu do có 0,06 mol Fe3+.
TH2: HNO3 dư.
=> 3x+2y+0,05.6=0,15.3
giải được x = y = 0,03.
→ n H N O 3 d ư = 0 , 03 . 2 - 0 , 03 3 . 4 = 0 , 04
Bảo toàn nguyên tố N: n H N O 3 = a = 0 , 04 + 0 , 15 + 0 , 03 . 3 + 0 , 03 . 2 - 0 , 05 . 2 = 0 , 24 m o l
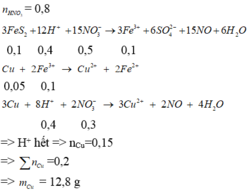
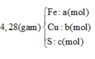

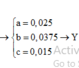
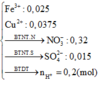
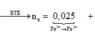
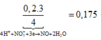
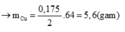


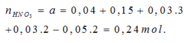
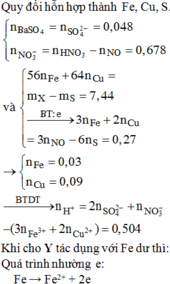


Đáp án : D
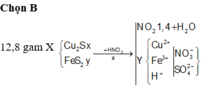
FeS2 + HNO3 -> Fe
FeS2 -> Fe3+ + 2S+6 + 15e
N+5 + 3e -> N+2
Bảo toàn e : 15 n F e S 2 = 3nNO
=> nNO = 0,75 mol
=> n N O 3 - s a u = 1,2 – 0,75 = 0,45 mol
Trong dung dịch sau có : Fe3+ ; H+ ; SO42- ; NO3-
Bảo toàn điện tích : 3.0,15 + nH+ = 2.0,3 + 0,45
=> n H + = 0,6 mol
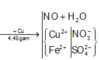
3Cu + 8H+ + 2NO3- -> 3Cu2+ + 2NO + 4H2O
2Fe3+ + Cu -> 2Fe2+ + Cu2+
=> nCu = 0,5 n F e 3 + + 3/8 n H + = 0,3 mol
=> m = 19,2g