Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
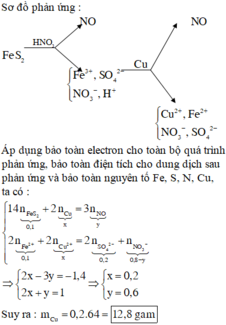
Sơ đồ phản ứng :
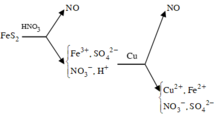
Áp dụng bảo toàn electron cho toàn bộ quá trình phản ứng, bảo toàn điện tích cho dung dịch sau phản ứng và bảo toàn nguyên tố Fe, S, N, Cu, ta có :
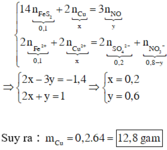

Chọn A
Quy đổi hỗn hợp về Fe (x mol); Cu (y mol) và S (z mol)
Bảo toàn S có
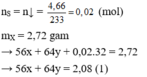
Do Y có thể hòa tan được Cu, bảo toàn electron có:
3 . n F e + 2 . n C u + 6 . n S = 3 . 0 , 07
→ 3x + 2y = 0,09 (2)
Từ (1) và (2) có: x = 0,02 và y = 0,015.
Dung dịch Y gồm: F e 3 + : 0,02 mol; C u 2 + : 0,015 mol; S O 4 2 - = 0,02 mol; N O 3 - = (0,5 – 0,07 = 0,43 mol) và có thể có H +
Bảo toàn điện tích → n H + = 0,38 mol
Cho Cu vào Y có phản ứng:
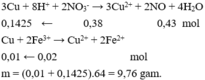

Đáp án B
![]()
Cho BaCl2 dư vào X thu được kết tủa là BaSO4
![]()
Quy đổi hỗn hợp về Fe x mol, Cu y mol và S 0,05 mol (bảo toàn S).
![]()
Bảo toàn e: ![]()
.giải ra nghiệm âm loại.
TH1: HNO3 hết thì X hòa tan được 0,03 mol Cu do có 0,06 mol Fe3+.
TH2: HNO3 dư.

Bảo toàn nguyên tố N:
![]()
![]()

Đáp án D
nS = nBaSO4= 0,024 => mFe + mCu = 2,496 (1)
nNO = 0,084; nHNO3 = 0,6
Bảo toàn N => nNO3 sau = nHNO3 – nNO = 0,516
Bảo toàn O => 3nHNO3 = nNO + 3nNO3 sau + 4nSO4 + nH2O => nH2O = 0,072
Bảo toàn H => nHNO3 = 2nH2O + nH+dư =>nH+dư = 0,456 => Chỉ tạo Fe3+
Bảo toàn ne => 3nFe + 2nCu + 6nS = 3nNO (2)
(1), (2) => nFe = 0,024; nCu = 0,018
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
Fe + Cu2+ → Fe2+ + Cu
Fe + 2Fe3+ → 3Fe2+
=> nFe = 0,375nH+dư + nCu2+ + 0,5nFe3+ = 0,201 => m = 11,256 => Chọn D.

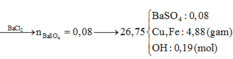
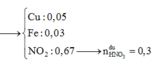
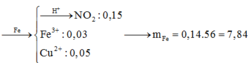


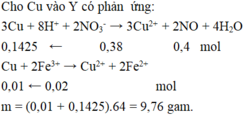

Đáp án A
0,1 mol FeS2 + 0,8 mol HNO3 → dd X + ↑NO x mol.
ddX + tối đa m gam Cu y mol.
- Bản chất của phản ứng là quá trình nhường, nhận electron:
FeS2 → Fe+2 + 2S+6 + 14e
Cu → Cu+2 + 2e
N+5O3- + 4H+ + 3e → N+2O + 2H2O
Theo bảo bảo electron: 14 × nFeS2 + 2 × nCu = 3 × nNO → 14 × 0,1 + 2y = 3x (*)
- Sau phản ứng trong dung dịch có Fe+2; Cu+2; NO3-; SO4-2
Theo bảo toàn điện tích 2 × nFe+2 + 2 × nCu+2 = 1 × nNO3- + nSO4-2
→ 2 × 0,1 + 2y = 3x + 0,1 × 2 (**)
Từ (*) và (**) → x = 0,6; y = 0,2 → mCu = 0,2 × 64 = 12,8 gam