Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2SO_4}=\dfrac{200.19,6}{100.98}=0,4mol\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ n_{CuSO_4\left(A\right)}=n_{CuO}=n_{H_2SO_4}=0,4mol\\ n_{Cu\left(OH\right)_2}=\dfrac{29,4}{98}=0,3mol\\ CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\\\Rightarrow\dfrac{0,4}{1}>\dfrac{0,3}{1}\Rightarrow CuSO_4.pư.không.hết\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
0,3mol 0,6mol 0,3mol
\(m_{ddB}=0,4.80+200+0,6.40-29,4=226,6g\\ C_{\%Na_2SO_4\left(B\right)}=\dfrac{0,3.142}{226,6}\cdot100=18,8\%\)

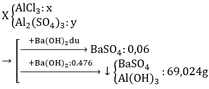
Cho Ba(OH)2 vào muối Al sẽ có 2TH sau:
TH1: kết tủa Al(OH)3 chưa bị hòa tan
Al3+ + 3OH– → Al(OH)3↓
→ nAl(OH)3 = nAl3+ → nAl(OH)3 = xn + 0,04n
TH2: kết tủa Al(OH)3 bị hòa tan một phần
Al3+ + 3OH– → Al(OH)3↓
(xn + 0,04n)→ 3(xn + 0,04n) (xn + 0,04n)
Al(OH)3 + OH– → AlO2– + 2H2O
0,952 – 3(xn + 0,04n) ←0,952
→ nAl(OH)3 = 4xn + 0,16n – 0,952


\(m_{NaOH\left(A\right)}=20.5\%=1\left(g\right)\)
Trong B:
gọi x là khối lượng Na2O thêm vào , x>0 (g)
\(10\%=\dfrac{\dfrac{80}{62}x+1}{x+20}\)
\(\rightarrow x=0,84\left(g\right)\)
Vậy khối Na2O thêm vào dd A là 0,84 (g)
b, \(m_{KOH\left(A\right)}=2\%.20=0,4\left(g\right)\)
\(C\%_{KOH\left(B\right)}=\dfrac{0,4}{20+0,84}.100\%=1,92\%\)

\(a)CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ b)n_{CuO}=\dfrac{4}{80}=0,05mol\\ n_{H_2SO_4}=\dfrac{100.20}{100.98}=\dfrac{10}{49}mol\\ \Rightarrow\dfrac{0,05}{1}< \dfrac{10:49}{1}\rightarrow H_2SO_4.dư\\ n_{CuSO_4}=n_{H_2SO_4}=n_{CuO}=0,05mol\\ C_{\%CuSO_4}=\dfrac{0,05.160}{100+4}\cdot100=7,69\%\\ C_{\%H_2SO_4}=\dfrac{\left(10:49-0,05\right)98}{100+4}\cdot100=14,52\%\)

Ta có: \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
PT: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
______0,2_____0,4_____0,2 (mol)
a, \(m_{CuCl_2}=0,2.135=27\left(g\right)\)
b, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\Rightarrow C\%_{HCl}=\dfrac{14,6}{300}.100\%\approx4,867\%\)
c, Ta có: m dd sau pư = 16 + 300 = 316 (g)
\(\Rightarrow C\%_{CuCl_2}=\dfrac{27}{316}.100\%\approx8,54\%\)

a) PTHH: \(Na_2O+H_2O\rightarrow2NaOH\)
Ta có: \(n_{NaOH}=2n_{Na_2O}=2\cdot\dfrac{6,2}{62}=0,2\left(mol\right)\) \(\Rightarrow C_{M_{NaOH}}=\dfrac{0,2}{0,4}=0,5\left(M\right)\)
b) PTHH: \(2NaOH+CuSO_4\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)
Ta có: \(\left\{{}\begin{matrix}n_{NaOH}=0,2\left(mol\right)\\n_{CuSO_4}=0,2\cdot2,5=0,5\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,5}{1}\) \(\Rightarrow\) CuSO4 còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{Cu\left(OH\right)_2}=0,1\left(mol\right)=n_{Na_2SO_4}\\n_{CuSO_4\left(dư\right)}=0,4\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Cu\left(OH\right)_2}=0,1\cdot98=9,8\left(g\right)\\C_{M_{Na_2SO_4}}=\dfrac{0,1}{0,4+0,2}\approx0,17\left(M\right)\\C_{M_{CuSO_4\left(dư\right)}}=\dfrac{0,4}{0,6}\approx0,67\left(M\right)\end{matrix}\right.\)
Ta có: \(n_{H_2SO_4}=\dfrac{200.19,6\%}{98}=0,4\left(mol\right)\)
\(n_{Cu\left(OH\right)_2}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PT: \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
Dung dịch A gồm: CuSO4 và H2SO4 dư
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
Đề có cho dữ kiện gì liên quan đến dd NaOH không bạn nhỉ?
cho mình hỏi là n H2SO4 là bạn sử dụng công thức
gì vậy