Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Cho 5,52 gam Mg, Al tác dụng với 0,54 mol NaHSO4 và 0,08 mol HNO3 thu được dung dịch X chỉ chứa muối trng hòa và hỗn hợp Y gồm 3 khí không màu
Ta có: M Y ¯ = 15 , 75
do vậy Y có H2, N2 và N2O
Cho NaOH dư vào X thu được kết tủa là Mg(OH)2
![]()
Do dung dịch X chứa chứa muối trung hòa nên H+ hết, mặt khác do sinh ra khí H2 nên NO3- hết.
Dung dịch X sẽ chứa Mg2+ 0,14 mol, Al3+ 0,08 mol, NH4+, Na+ 0,54 mol và SO42-0,54 mol.
Bảo toàn điện tích: ![]()
Bảo toàn N:
![]()
Gọi số mol N2, N2O và H2 lần lượt là a, b,c => a + b = 0,03
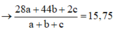
Bảo toàn e: 10a + 8b + 2c + 0,02.8 = 0,14.x + 0,08.3
Giải hệ: a=0,01; b=0,02; c=0,05
→ % H 2 = 7,94%

Chọn đáp án B
gt ⇒ Z gồm N2O, N2, H2 ⇒ Y không chứa NO3–; khí có PTK lớn nhất trong Z là N2O.
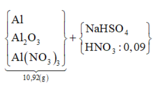
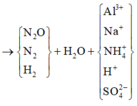
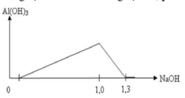
Từ 1 mol NaOH đến 1,3 mol NaOH thì kết tủa từ cực đại đến tan hết do xảy ra phản ứng:
Al(OH)3 + NaOH → NaAlO2 + 2H2O ⇒ nAl3+ = nAl(OH)3 = 1,3 - 1 = 0,3 mol.
Đặt nNaHSO4 = x ⇒ nNa+/Y = nSO42– = x. Khi kết tủa đạt cực đại thì chỉ thu được Na2SO4.
⇒ nNa2SO4 = x ⇒ ∑nNa+ = 2x ⇒ nNa+/Y = 2x - 1 = x ⇒ x = 1.
Đặt nNH4+ = y; nH+ = z. Bảo toàn điện tích: 0,3 × 3 + 1 + y + z = 1 × 2
mmuối = 127,88(g) = 0,3 × 27 + 1 × 23 + 18y + z + 1 × 96
Giải hệ có: y = 0,04 mol; z = 0,06 mol. Bảo toàn khối lượng:
mH2O = 10,92 + 1 × 120 + 0,09 × 63 - 127,88 - 0,08 × 20 = 7,11g ⇒ nH2O = 0,395 mol.
Bảo toàn nguyên tố Hidro: nH2 = (1 + 0,09 - 0,04 × 4 - 0,06 - 0,395 × 2)/2 = 0,04 mol.
Đặt nN2O = a; nN2 = b ⇒ nZ = a + b + 0,04 = 0,08; mZ = 44a + 28b + 0,04 × 2 = 0,08 × 20
Giải hệ có: a = 0,025 mol; b = 0,015 mol ⇒ %mN2O = 0,025 × 44 ÷ 1,6 × 100% = 68,75%.

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

A. 184,1 gam và 91,8 gam.
B. 84,9 gam và 91,8 gam.
C. 184,1 gam và 177,9 gam.
D. 84,9 gam và 86,1 gam.

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến

Đáp án B
Z chắc chắn phải chứa CO2. Lại có MZ = 44 = MCO2 ⇒ khí còn lại cũng có M = 44.
⇒ Khí còn lại là N2O || NaOH + Y → ↓ rồi nung ⇒ chỉ có MgO ⇒ nMg2+ = 0,34 mol.
► Ta có sơ đồ sau:

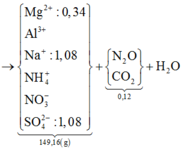
Bảo toàn khối lượng: mH2O = 11,16(g) ⇒ nH2O = 0,62 mol. Bảo toàn nguyên tố Hidro:
⇒ nNH4+ = (1,08 + 0,32 - 0,62 × 2) ÷ 4 = 0,04 mol || Đặt nAl3+ = x; nNO3– = y
⇒ mmuối = 27x + 62y + 137,4 = 149,16(g) || Bảo toàn điện tích: 3x - y = 0,36 mol.
► Giải hệ có: x = 0,16 mol; y = 0,12 mol. Bảo toàn nguyên tố Nitơ: nN2O = 0,08 mol.
⇒ nMgCO3 = nCO2 = 0,04 mol. Bảo toàn nguyên tố Mg: nMg = 0,32 mol.
● ∑nH+ = 10nNH4+ + 10nN2O + 2nO + 2nCO3 ⇒ nO = 0,06 mol
⇒ nAl2O3 = 0,02 mol ||⇒ %mAl2O3 = 0,02 × 102 ÷ 15,84 × 100% = 12,88%

 với các chất sau:
với các chất sau:
Đáp án B
Cho 5,52 gam Mg, Al tác dụng với 0,54 mol NaHSO4 và 0,08 mol HNO3 thu được dung dịch X chỉ chứa muối trng hòa và hỗn hợp Y gồm 3 khí không màu
Ta có: M Y ¯ = 15 , 75
do vậy Y có H2, N2 và N2O
Cho NaOH dư vào X thu được kết tủa là Mg(OH)2
→ n M g = 0 , 14 → n A l = 0 , 08 m o l
Do dung dịch X chứa chứa muối trung hòa nên H+ hết, mặt khác do sinh ra khí H2 nên NO3- hết.
Dung dịch X sẽ chứa Mg2+ 0,14 mol, Al3+ 0,08 mol, NH4+, Na+ 0,54 mol và SO42-0,54 mol.
Bảo toàn điện tích: n N H 4 + = 0 , 02 m o l
Bảo toàn N:
Gọi số mol N2, N2O và H2 lần lượt là a, b,c
Bảo toàn e:
Giải hệ: a=0,01; b=0,02; c=0,05