Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{NaOH}=0,1.1,54=0,154\left(mol\right)\)
Gọi: V dd Y = a (l) \(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,2a\left(mol\right)\\n_{AlCl_3}=0,3a\left(mol\right)\end{matrix}\right.\)
PT: \(NaOH+HCl\rightarrow NaCl+H_2O\) (1)
\(3NaOH+AlCl_3\rightarrow3NaCl+Al\left(OH\right)_{3\downarrow}\) (2)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\) (3)
a, - Kết tủa trắng bắt đầu xuất hiện khi pư (1) vừa kết thúc.
Theo PT: \(n_{NaOH}=n_{HCl}\Rightarrow0,154=0,2a\Rightarrow a=0,77\left(l\right)=770\left(ml\right)\)
b, - Kết tủa trắng lớn nhất khi pư (2) vừa kết thúc.
Theo PT: \(n_{NaOH}=n_{HCl}+3n_{AlCl_3}\Rightarrow0,154=0,2a+3.0,3a\Rightarrow a=0,14\left(l\right)=140\left(ml\right)\)
c, Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{1,638}{78}=0,021\left(mol\right)\)
- TH1: Kết tủa chưa bị hòa tan.
Theo PT: \(n_{NaOH}=n_{HCl}+3n_{Al\left(OH\right)_3}\Rightarrow0,154=0,2a+3.0,021\Rightarrow a=0,455\left(l\right)=455\left(ml\right)\)
- TH2: Kết tủa đã bị hòa tan một phần.
Theo PT: \(n_{Al\left(OH\right)_3\left(2\right)}=n_{AlCl_3}=0,3a\left(mol\right)\)
\(\Rightarrow n_{Al\left(OH\right)_3\left(3\right)}=0,3a-0,021\left(mol\right)\)
\(\Rightarrow n_{NaOH}=n_{HCl}+3n_{AlCl_3}+n_{Al\left(OH\right)_3\left(3\right)}\)
\(\Rightarrow0,154=0,2a+3.0,3a+0,3a-0,021\Rightarrow a=0,125\left(l\right)=125\left(ml\right)\)
d, \(n_{NaOH}=0,1.1,5=0,15\left(mol\right)\)
PT: \(HCl+NaOH\rightarrow NaCl+H_2O\)
____x________x (mol)
\(AlCl_3+4NaOH\rightarrow NaAlO_2+3NaCl+2H_2O\)
y___________4y_______y (mol)
\(HCl+NaAlO_2+H_2O\rightarrow Al\left(OH\right)_{3\downarrow}+NaCl\)
z_________z (mol)
\(AlCl_3+3NaAlO_2+6H_2O\rightarrow4Al\left(OH\right)_{3\downarrow}+3NaCl\) (*)
b___________3b (mol)
\(3HCl+Al\left(OH\right)_3\rightarrow AlCl_3+3H_2O\)
- Thu được tủa bền, không tan khi lắc dd khi vừa kết thúc pư (*)
Theo PT: x + 4y = 0,15 và z + 3b = y ⇒ x + 4y + z + 3b = 0,15 + y ⇒ (x + z) + 3.(y + b) = 0,15
Mà: x + z = 0,2a
y + b = 0,3a
⇒ 0,2a + 3.0,3a = 0,15 ⇒ a = 3/22 (l) = 1500/11 (ml)

Để xác định nồng độ của dung dịch X và Y, chúng ta cần sử dụng phương pháp giải phương trình hóa học và áp dụng định luật bảo toàn khối lượng.
Phương trình hóa học cho phản ứng giữa AlCl3 và NaOH là:
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
Theo định luật bảo toàn khối lượng, khối lượng của chất tham gia phản ứng bằng khối lượng của chất sản phẩm. Ta có thể xác định khối lượng của kết tủa Al(OH)3 trong mỗi trường hợp.
Trong trường hợp thứ nhất, thêm từ từ 200 ml dung dịch Y vào 200 ml dung dịch X, thu được 15.6 gam kết tủa. Vì vậy, khối lượng của Al(OH)3 trong trường hợp này là 15.6 gam.
Trong trường hợp thứ hai, thêm từ từ 200 ml dung dịch Y vào 100 ml dung dịch X, thu được 10.92 gam kết tủa. Vì lượng chất tham gia phản ứng là gấp đôi so với trường hợp thứ nhất, khối lượng của Al(OH)3 trong trường hợp này cũng gấp đôi, tức là 21.84 gam.
Giờ chúng ta có thể xác định nồng độ của dung dịch X và Y. Để làm điều đó, ta cần biết công thức phân tử của Al(OH)3 và khối lượng mol của nó. Al(OH)3 có công thức phân tử là Al(OH)3, tức là mỗi phân tử Al(OH)3 có khối lượng là 78 g/mol.
Trong trường hợp thứ nhất, dung dịch X và Y có tỉ lệ 1:1, vì vậy dung dịch X có khối lượng mol AlCl3 là 15.6/78 = 0.2 mol. Vì dung dịch X có thể làm kết tủa hết 0.2 mol AlCl3, nồng độ của dung dịch X là 0.2 mol/0.2 L = 1 M.
Trong trường hợp thứ hai, dung dịch X và Y có tỉ lệ 1:2, vì vậy dung dịch X có khối lượng mol AlCl3 là 21.84/78 = 0.28 mol. Vì dung dịch X có thể làm kết tủa hết 0.28 mol AlCl3, nồng độ của dung dịch X là 0.28 mol/0.1 L = 2.8 M.
Vậy, nồng độ của dung dịch X và Y lần lượt là 1 M và 2.8 M.

Gọi số mol K, Ba là a, b (mol)
PTHH: 2K + 2H2O --> 2KOH + H2
a--------------->a---->0,5a
Ba + 2H2O --> Ba(OH)2 + H2
b-------------->b----->b
=> \(0,5a+b=\dfrac{0,392}{22,4}=0,0175\left(mol\right)\) (1)
Kết tủa thu được là BaCO3
\(n_{BaCO_3}=\dfrac{0,985}{197}=0,005\left(mol\right)\)
=> nBa = 0,005 (mol)
=> b = 0,005 (mol) (2)
(1)(2) => a = 0,025 (mol); b = 0,005 (mol)
\(\left\{{}\begin{matrix}\%m_K=\dfrac{0,025.39}{0,025.39+0,005.137}.100\%=58,735\%\\\%m_{Ba}=\dfrac{0,005.137}{0,025.39+0,005.137}.100\%=41,265\%\end{matrix}\right.\)
Y gồm \(\left\{{}\begin{matrix}KOH:0,025\left(mol\right)\\Ba\left(OH\right)_2:0,005\left(mol\right)\end{matrix}\right.\)
Gọi công thức chung của bazo là XOH
nXOH = 0,025 + 0,005.2 = 0,035 (mol)
\(n_{AlCl_3}=0,1.0,1=0,01\left(mol\right)\)
PTHH: 3XOH + AlCl3 --> 3XCl + Al(OH)3
Xét tỉ lệ: \(\dfrac{0,035}{3}>\dfrac{0,01}{1}\) => AlCl3 hết
PTHH: 3XOH + AlCl3 --> 3XCl + Al(OH)3
0,01----------->0,01
=> mAl(OH)3 = 0,01.78 = 0,78 (g)

Gọi \(\left\{{}\begin{matrix}n_{Na_2O}=a\left(mol\right)\\n_{Al_2O_3}=b\left(mol\right)\end{matrix}\right.\)
nHCl = 0,2.0,2 = 0,04 (mol)
PTHH: \(Na_2O+H_2O\rightarrow2NaOH\)
_______a--------------------->2a______(mol)
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
__b--------->2b------------>2b_________(mol)
Do trong dung dịch chứa 2 chất tan có cùng nồng độ mol
=> nNaOH = nNaAlO2 => 2a - 2b = 2b => a = 2b
PTHH: NaOH + HCl \(\rightarrow\) NaCl + H2O
______0,04<----0,04________________(mol)
=> 2a - 2b = 0,04
=> a = 0,04 (mol) ; b = 0,02 (mol)
=> m = \(0,04.62+0,02.102=4,52\left(g\right)\)

nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
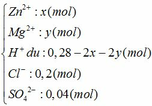
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
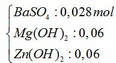
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

$n_{OH^-} = 0,5.1,5 + 0,5.1 = 1,25(mol)$
$n_{Zn^{2+}} = 0,5.0,25 + 0,5.0,75 = 0,5(mol)$
Zn2+ + 2OH- → Zn(OH)2
0,5...............1....................0,5............(mol)
Zn(OH)2 + 2OH- → ZnO22- + 2H2O
0,125...............0,25...............................................(mol)
Suy ra: $m = (0,5 - 0,125).99 = 37,125(gam)$

nK2CO3=nNaHCO3=amol;nBa(HCO3)2=bmol
->nCO2−3=amol
->nHCO−3=(a+2b)mol
2H++CO2−3→CO2↑+H2O
H++HCO−3→CO2↑+H2O
nHCl=0,5.0,56=0,28mol→2a+(a+2b)=0,28(1)
HCO−3+OH−→CO2−3+H2O
nNaOH=0,2.1=0,2mol→a+2b=0,2(2)
(1),(2)→a=0,04;b=0,08
K2CO3+Ba(HCO3)2→BaCO3↓+2KHCO3
0,04 0,08 → 0,04
mBaCO3=0,04.197=7,88g
Copy thiếu kìa