Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bạn bấn vào đây, có người hỏi bài này rồi nhá Câu hỏi của Mạc Nhược Ca - Hóa học lớp 12 | Học trực tuyến

Đáp án C
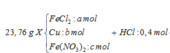
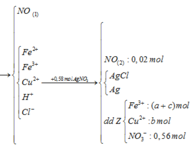
Vì dd Y + AgNO3 thoát ra khí NO => trong Y phải có H+ dư và Fe2+
4H+ + NO3- + 3e→ NO + 2H2O
0,4 → 0,1 (mol)
=> nNO(1) = ∑ nNO – nNO(2) = 0,1 – 0,02 = 0,08 (mol)
BTNT N : nFe(NO3)2 = 1/2 nNO(1) = 0,08/2 = 0,04 (mol) = c (1)
BTKL: mX = 127a + 64b +180c = 23,76 (2)
BTĐT đối với dd Z : 3(a+c) +2b = 0,56 (3)
Từ (1), (2) và (3) => a = 0,08 (mol); b = 0,1 (mol); c = 0,04 (mol)
BTNT Cl: nAgCl = nCl- = 2a+ 0,4 = 2.0,08 + 0,4 = 0,56 (mol)
BTNT Ag: nAg = ∑ nAgCl – nAgCl = 0,58 – 0,56 = 0,02 (mol)
=> Khối lượng kết tủa: m↓ = mAgCl + mAg = 0,56.143,5 + 0,02.108 = 82,52 (g)
Gần nhất với 82 gam

N+5 +1e =>N+4
0,02 mol<=0,02 mol
2N+5 +2.4e =>2N+1
0,04 mol<=0,01 mol
ne nhận=ne nhường=0,06 mol
nNO3- tạo muối=ne nhận=0,06 mol
=>mNO3-=0,06.62=3,72g
mKL=5,04g=>m muối=m gốc KL+mNO3-=3,72+5,04=8,76g
nHNO3 =0,06+0,02+0,005.2=0,09 mol
=>CM dd HNO3=0,09/0,1=0,9M
Phương trình nhận electron:
N+5 + 8e → N2O
N+5 +1e→NO2
nNO tạo muối = nNO + 8nN2O = 0,02 + 8.0,005 = 0.02 + 0,04 = 0,06 mol
mNO tạo muối =0,06.62 = 3,72g
m =mKL+ mNO tạo muối = 5,04 + 3,72 = 8,76g
nHNO3 tham gia phản ứng = 2nNO + 10nN2O = 2.0,02 + 10.0,005= 0,09 mol
x =0.09:0,1=0,9M ==>> Đáp án thứ nhất

Đáp án C
Do Y tác dụng AgNO3 sinh ra NO ⇒ trong Y có chứa H+ và NO3– hết.
4H+ + NO3– + 3e → NO + 2H2O ⇒ ở phản ứng đầu, nH+ = 0,4 – 0,02 × 4 = 0,32 mol.
⇒ nNO3– = 0,32 ÷ 4 = 0,08 mol ⇒ nFe(NO3)2 = 0,04 mol.
Đặt nFeCl2 = x mol; nCu = y mol. mX = 127x + 64y + 0,04 × 180 = 23,76 gam.
Bảo toàn nguyên tố Clo : nAgCl = 2x + 0,4 mol.
Bảo toàn nguyên tố Ag : nAg = 0,58 – (2x + 0,4) = 0,18 – 2x mol.
Bảo toàn electron cả quá trình : nFeCl2 + 2nCu + nFe(NO3)2 = nAg + 3/4nH+.
⇒ x + 2y + 0,04 = 0,18 – 2x + 3/4 × 0,4 ⇒ giải: x = 0,08 mol; y = 0,1 mol.
⇒ nAg = 0,02 mol; nAgCl = 0,56 mol ⇒ m = 0,02 × 108 + 0,56 × 143,5 = 82,52 gam.
Cách khác: nNO = nH+ ÷ 4 = 0,4 ÷ 4 = 0,1 mol.
Bảo toàn nguyên tố Nitơ: nNO3– = 0,04 × 2 + 0,58 – 0,1 = 0,56 mol.
Bảo toàn nguyên tố Fe: nFe3+ = x + 0,04 mol.
Bảo toàn điện tích: (x + 0,04) × 3 + 2y = 0,56 mol ⇒ x và y
⇒ giải tương tự như cách trên!

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.

 với các chất sau:
với các chất sau:
Đáp án C
Vì dd Y + AgNO3 thoát ra khí NO => trong Y phải có H+ dư và Fe2+
4H+ + NO3- + 3e→ NO + 2H2O
0,4 → 0,1 (mol)
=> nNO(1) = ∑ nNO – nNO(2) = 0,1 – 0,02 = 0,08 (mol)
BTNT N : nFe(NO3)2 = 1/2 nNO(1) = 0,08/2 = 0,04 (mol) = c (1)
BTKL: mX = 127a + 64b +180c = 23,76 (2)
BTĐT đối với dd Z : 3(a+c) +2b = 0,56 (3)
Từ (1), (2) và (3) => a = 0,08 (mol); b = 0,1 (mol); c = 0,04 (mol)
BTNT Cl: nAgCl = nCl- = 2a+ 0,4 = 2.0,08 + 0,4 = 0,56 (mol)
BTNT Ag: nAg = ∑ nAgCl – nAgCl = 0,58 – 0,56 = 0,02 (mol)
=> Khối lượng kết tủa: m↓ = mAgCl + mAg = 0,56.143,5 + 0,02.108 = 82,52 (g)
Gần nhất với 82 gam