Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
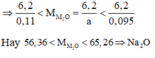
Đáp án B

Gọi kim loại là M ta có
PTHH: MxOy + y H2 xM + yH2O
8(g) 3,36 lít
8:(Mx+16y) 0,15 (0,15x):y 0,15 (mol)
PTHH2: M + 2xHCl -> MClx + xH2
(0,15x):y 0,1 mol
Ta thấy nM=(0,15.x):(x.y)=0.15:y mol và 0.15:y=8:(Mx+16y)
Rút ra x/y=2/3 và M=56
Vậy đó là Fe2O3

\(CT:M\left(OH\right)_n\)
\(M\left(OH\right)_n+nHCl\rightarrow MCl_n+nH_2O\)
\(M+17n...........M+35.5n\)
\(7.4..........................11.37\)
\(\Leftrightarrow11.37\left(M+17n\right)=7.4\left(M+35.5n\right)\)
\(\Leftrightarrow3.97M-69.41n=0\)
\(\Leftrightarrow M=17.48n\)
\(n=3\Rightarrow M=52\)
\(CT:Cr\left(crom\right)\)


Giải hệ 3 phương trình 3 ẩn trên ta được:
a = 0,2 mol; k = 0,15
→ m2= 0,15m1
→ m = 1,15.m1 = 57,5g


nM2O=\(\frac{9,4}{2M+16}\) (mol)
- p1 làm quỳ hoá xanh → OH- dư → nOH->nHCl=0,095 (mol)
- p2 làm quỳ hoá đỏ → H+ dư → nHCl>nOH-=0,105 (mol)
\(\Rightarrow0,105\cdot2>\frac{9,4}{2M+16}>0,095\cdot2\)
\(\Leftrightarrow41,474>M>31,14\)
→ M=39 (K) →K2O
nhầm p2 H+ dư → nHCl=0,105 >nOH-