Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Fe}:n_{Zn}=1:1\) \(\Rightarrow n_{Fe}=n_{Zn}\)
Theo PTHH, ta có: \(n_{Fe}=n_{Zn}=\dfrac{0,4}{2}=0,2mol\)
\(m_{Fe}=0,2.56=11,2g\)
\(m_{Zn}=0,2.65=13g\)
\(\%m_{Fe}=\dfrac{11,2}{11,2+13}.100=46,28\%\)
\(\%m_{Zn}=100\%-46,28\%=53,72\%\)
\(n_{Fe}:n_{Zn}=1:1\) là đầu bài cho mà :)
Đáng ra đúng là: Theo pthh: \(n_{hhkl\left(Fe,Zn\right)}=n_{H_2}=0,4\left(mol\right)\) chứ, em đã tính cái này đâu

PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
a____________________a (mol)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
b___________________b (mol)
Ta lập hệ phương trình: \(\left\{{}\begin{matrix}24a+56b=10,4\\a+b=\dfrac{6,72}{22,4}=0,3\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=0,2\cdot24=4,8\left(g\right)\\m_{Fe}=5,6\left(g\right)\end{matrix}\right.\)
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt : Mg + 2HCl → MgCl2 + H2\(|\)
1 2 1 1
a 2a 0,3
Fe + 2HCl → FeCl2 + H2\(|\)
1 2 1 1
b 2b 0,3
Gọi a là số mol của Mg
b là số mol của Fe
Theo đề ta có : mMg + mFe = 10,4 (g)
⇒ nMg . MMg + nFe . MFe = 10,4 g
24a + 56b = 10,4 g (1)
Theo phương trình : 1a + 1b = 0,3 (2)
Từ (1),(2) , ta có hệ phương trình : 24a + 56b = 10,4
1a + 1b = 0,3
⇒ \(\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
Khối lượng của magie
mMg = nMg. MMg
= 0,2 .24
= 4,8 (g)
Khối lượng của sắt
mFe = nFe . MFe
= 0,1. 56
= 5,6 (g)
Chúc bạn học tốt

\(a,A+2HCl\rightarrow ACl_2+H_2\\ n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\Rightarrow n_A=n_{H_2}=0,15\left(mol\right)\\ \Rightarrow M_A=\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow A\left(II\right):Magie\left(Mg=24\right)\\ b,Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\\ Vì:\dfrac{0,15}{1}< \dfrac{0,4}{2}\Rightarrow HCldư\\ \Rightarrow Sau.p.ứ:MgCl_2,HCldư\\ n_{MgCl_2}=n_{Mg}=0,15\left(mol\right)\\ \Rightarrow m_{MgCl_2}=95.0,15=14,25\left(g\right)\\ n_{HCl\left(dư\right)}=0,4-0,15.2=0,1\left(mol\right)\\ \Rightarrow m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\\ m_{chất.sau}=3,65+14,25=17,9\left(g\right)\)

PTHH: Zn + 2HCl \(\rightarrow\) ZnCl2 + H2\(\uparrow\)(1)
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2\(\uparrow\)(2)
Gọi x,y lần lượt là số mol của Zn , Al có trong 15,7g hh(x,y>0)
Theo PT(1): nHCl = 2nZn = 2x(mol)
Theo PT(2): nHCl = 3nAl = 3y(mol)
Vì nHCl = \(\frac{200.3,5}{1000}=0,7\left(mol\right)\)
=> nHCl(1) + nHCl(2)= 0,7
=>2x+3y = 0,7 (*)
Theo đề, ta có:mZn+mAl=15,7
=> 65x+27y=15,7(**)
Từ (*)và (**)=>\(\left\{{}\begin{matrix}65x+27y=15,7\\2x+3y=0,7\end{matrix}\right.\)=> \(\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
Vậy khối lượng mỗi kim loại trong hh ban đầu lần lượt là:
mZn = 0,2.65=13(g)
mAl = 15,7-13 = 2,7(g)

Ta có: mCu = 1,86 (g)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Có: mAl + mFe = 6 - 1,86 = 4,14 (g)
Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 4,14 (1)
Ta có: \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{3}{2}x+y\left(mol\right)\)
\(\Rightarrow\dfrac{3}{2}x+y=0,135\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,06\left(mol\right)\\y=0,045\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{1,86}{6}.100\%=31\%\\\%m_{Al}=\dfrac{0,06.27}{6}.100\%=27\%\\\%m_{Fe}=42\text{%}\end{matrix}\right.\)
Bạn tham khảo nhé!
Chất rắn không tan sau phản ứng là Cu
=> m Cu = 1,86(gam)
Gọi n Al =a (mol) ; n Fe = b(mol) => 27a + 56b = 6 -1,86 = 4,14(1)
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
n H2 = 1,5a + b = 3,024/22,4 = 0,135(2)
Từ (1)(2) suy ra a = 0,06 ; b = 0,045
Vậy :
%m Cu = 1,86/6 .100% = 31%
%m Al = 0,06.27/6 .100% = 27%
%m Fe = 100% -31% -27% = 42%

Chào em, bài này rất dễ ko cần giải, nhìn là biết đáp án ngay, giải chi mất thời gian. Anh phân tích cho nha:
- thứ nhất : X là hợp chất của A với oxi(A hóa trị 2) => cthh của X là : AO
-thứ 2 : PTK của X là 80 đvC, biết PTK của oxi là 16
=> từ (1) và (2) suy ra NTK của A = MX - MO= 80-16=64.Vậy A là Cu -> CTHH của X là CuO
nếu trắc nghiệm thì làm vậy để tiết kiệm thời gian. Bài rất dễ em muốn giải chi tiết ra cũng được.
Chúc em học tốt.!!! Có gì liên lạc với anh nha:))

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 ( mol )
( Cu không tác dụng với dd axit HCl )
\(m_{Fe}=0,1.56=5,6g\)
\(\rightarrow m_{Cu}=12-5,6=6,4g\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{12}.100=46,66\%\\\%m_{Cu}=100\%-46,66\%=53,34\%\end{matrix}\right.\)
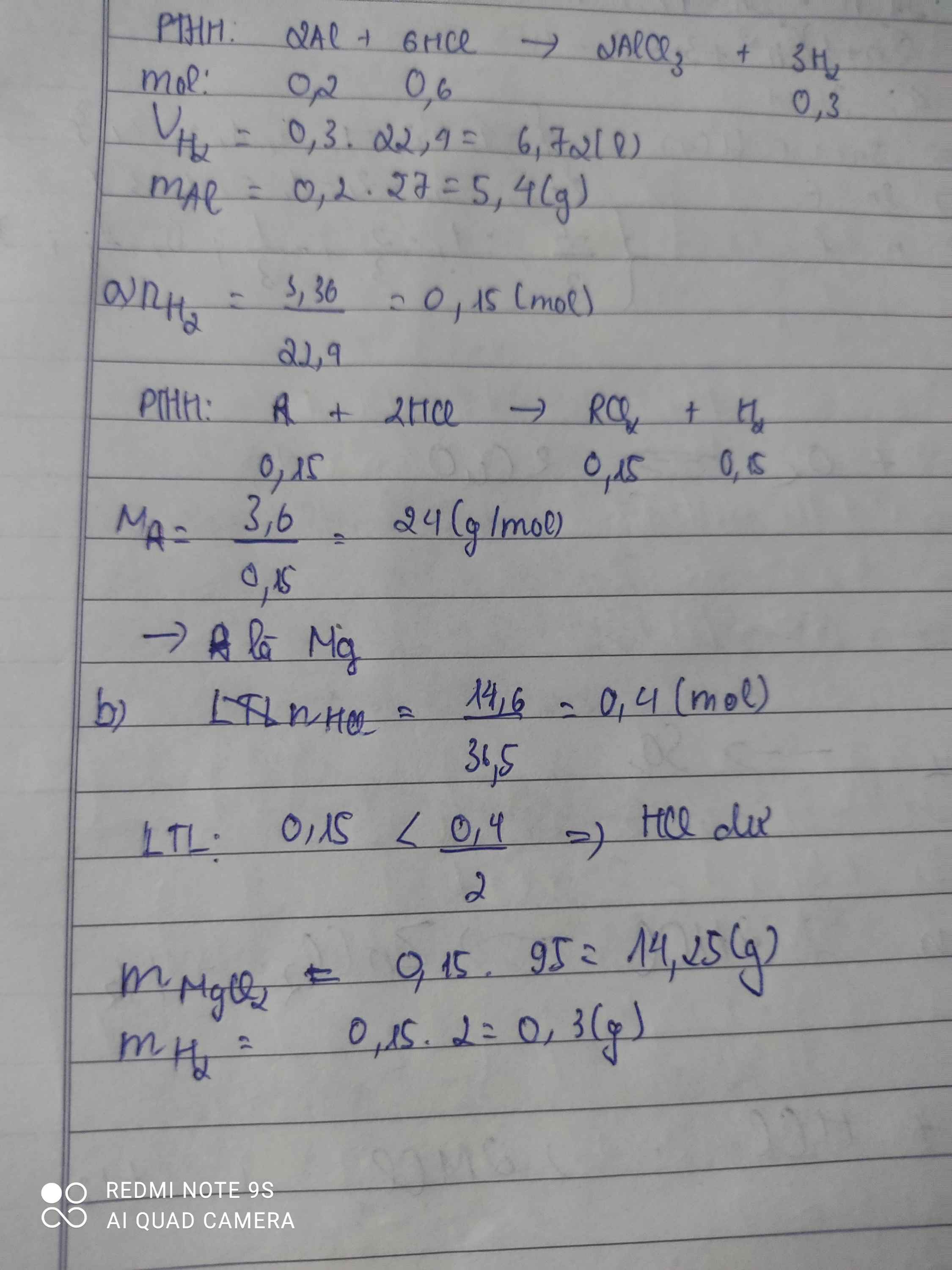
do cho thêm axit mà vẫn dư thì axit sẽ td kết kim loại đó mà còn 2 g chất ko tan có thể là cặn hoặc Cu, Ag,Auvv