Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta đặt: nNO= x mol; nNO2= y mol
Ta có : nY= x+y= 6,72/22,4= 0,3 mol
mY= 30x+ 46y= nY.MY= 0,3.19.2
Giải hệ có x= 0,15 và y= 0,15
Đặt nFe= a mol ; nCu= b mol
QT cho e:
Fe → Fe3++ 3e
a 3a mol
Cu → Cu2++ 2e
b 2b mol
QT nhận e:
N+5+ 3e→ NO
0,45 0,15
N+5+ 1e→ NO2
0,15 0,15
Theo ĐL bảo toàn e có: ne cho= ne nhận nên 3a+2b= 0,45+ 0,15= 0,60
Mặt khác mkim loại= 56a+ 64b= 15,2
Giải hệ trên có a= 0,1, b= 0,15 →%mFe=36,84%
Đáp án C

X+ HNO3→ Dung dịch D
Dung dịch D + NaOH→ Khí
→Dung dịch D phải có NH4NO3
NH4NO3+ NaOH → NaNO3+ NH3↑ + H2O
0,3← 0,3 mol
QT nhận e:
NO3-+ 8e+ 10H+ → NH4+ + 3H2O (3)
2,4 0,3 mol
ne nhận= 8nNH4+= 2,4 mol
QT cho e: Gọi số oxi hóa cao nhất của kim loại M là n (n=1,2,3)
M → Mn++ ne
Theo ĐLBT e : necho= ne nhận nên ne cho= 2,4 mol → nM= 2,4/ n mol
→MM= mM: nM= 21,6: 2,4/n=9n
Thay các giá trị n và M ta thấy chỉ có n=3, M=27 thỏa mãn
Vậy M là Al.
Đáp án B

\(\left\{{}\begin{matrix}n_{Cu}\\n_{Fe}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}64x+56y=24,4\\2x+3y=\dfrac{6,72}{22,4}.3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,285\\y=0,11\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Cu}=74,75\%\\\%m_{Fe}=25,25\%\end{matrix}\right.\)

Mol SO2=2,688/22,4=0,12 mol
M \rightarrow M+2 +2e
0,12 mol<= 0,24 mol
S+6 +2e \rightarrow S+4
0,24 mol<=0,12 mol
=>0,12M=7,68=>M=64 M là Cu
b) mol O2=2,24/22,4=0,1 mol
Mol hhB=4,256/22,4=0,19 mol
2SO2 + O2 \rightleftharpoons 2SO3
Bđ:0,12 mol;0,1 mol
Pứ::x mol=>0,5x mol=>x mol
Sau:0,12-x mol;0,1-0,5x mol;x mol
Molhh B=0,12-x+0,1-0,5x+x=0,19=>x=0,06 mol
Vậy hh B gồm 0,06 mol SO2 0,07 mol O2 0,06 mol SO3 =>%V
c) mol Fe=6,72/56=0,12 mol
Mol Cu=7,84/64=0,1225 mol
mcr sau pứ=8,8g>mCu=>Cu chưa pư vs axit, Fe pứ 1phần
Fe \rightarrow Fe+3 +3e
x mol. => 3x mol
S+6 +2e \rightarrow S+4
3x mol=>1,5x mol
2Fe3+ + Fe \rightarrow 3Fe2+
x mol=>0,5 x mol
Fe dư:0,12-1,5x mol=>mFe=6,72-84x
mcr=8,8=6,72-84x+7,84=>x=0,06857 mol=>mol SO2=0,103 mol=>V=2,304l

Ta có: \(n_{H_2}=\dfrac{0,5376}{22,4}=0,024\left(mol\right)\)
\(n_{OH^-}=2n_{H_2}=0,048\left(mol\right)\)
Gọi: \(\left\{{}\begin{matrix}n_{H_2SO_4}=x\left(mol\right)\\n_{HCl}=2x\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H^+}=2n_{H_2SO_4}+n_{HCl}=2x+2x=4x\left(mol\right)\)
PT: \(H^++OH^-\rightarrow H_2O\)
\(\Rightarrow4x=0,048\Rightarrow x=0,012\left(mol\right)\)
⇒ nSO42- = nH2SO4 = 0,012 (mol)
nCl- = nHCl = 0,024 (mol)
⇒ m muối = mKL + mSO42- + mCl- = 1,788 + 0,012.96 + 0,024.35,5 = 3,792 (g)
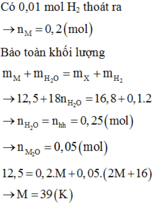



\(n_{H_2}=0,3\left(mol\right)\)
\(n_X=\dfrac{7,2}{X}\left(mol\right)\)
PTHH: \(2X+nH_2SO_4\rightarrow X_2\left(SO_4\right)_n+nH_2\)
Theo PTHH: \(\dfrac{0,6}{n}=\dfrac{7,2}{X}\Rightarrow X=12n\)
\(n=2\Rightarrow X=24\left(Mg\right)\)
nH2 = 6,72/22,4 = 0,3 mol
X + 2HCl -> XCl2 + H2
=>nX=nH2=0,3 mol
=>MX=7,2/0,3=24
=>X là Mg