
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

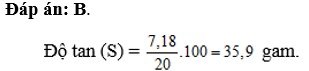

1. Khối lượng chất tan trong dung dịch 1 = m1C1/100 (g)
Khối lượng chất tan trong dung dịch 2 = m2C2/100 (g).
mà (m3 = m1 + m2)
Khối lượng chất tan trong dung dịch 3 = (m1 + m2)C3/100 (g).
Áp dụng định luật bảo toàn khối lượng ta có: C3.(m1 + m2) = C1.m1 + C2.m2
2. Đặt công thức của muối là: MgSO4.nH2O
Khối lượng MgSO4 trong dung dịch ban đầu: 200.35,1/135,1 = 51,961 gam
Ở 20oC:
- 135,1 gam dung dịch có chứa 35,1 gam MgSO4
- (200+2 – m) gam dung dịch có chứa (51,961 + 2 – 3,16) gam MgSO4.
Từ đó tìm được m = 6,47 gam
Khi nung muối ta có:
MgSO4.nH2O → MgSO4 + nH2O (1)
Theo (1) ta được mH2O = 6,47 – 3,16 = 3,31 gam
=> 3,16/120.18n = 3,31 => n = 7
Vậy muối là: MgSO4.7H2O
tham khảo nhé

ChọnC
- Độ tan (S) của một chất trong nước là số gam chất đó hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa ở một nhiệt độ xác định.
150 gam nước hòa tan được 10,95 gam KN O 3
100 gam nước hòa tan được S gam KN O 3
=> độ tan S = 100.10,95 150 = 7,3 g

a/ Xác định kim loại M
nH2SO4 ban đầu = 78,4.6,25:100=0.05 mol
Goi số mol MO là a mol, mMO = (M+16).a
MO+H2SO4---MSO4+H2O(1)
a mol amol amol
Số mol axit dư sau phản ứng (1): 0,05-a mol
mdd sau phản ứng: (m+16)a+78,4
Theo bài ra ta có: 2,433=100.(0,05-a).98/[(m+16)a+78,4] (I)
Mặt khác: MO+CO---M+CO2 (2)
a mol a mol a mol amol
Theo bài ra CO2 tham gia phản ứng hết, các phản ứng có thể xảy ra:
CO2+2NaOH--->Na2CO3+H2O
b 2b b b
CO2+NaOH--->NaHCO3
c c c
Khối lượng muối tạo thành: 100b+84c=2,96
- Nếu NaOH dư không xảy ra phản ứng (3). Tức là c = 0 mol,
b = a = 2,96 : 106 = 0,028 mol. Thay a = 0,028 vào (I) ta tìm được M = 348,8 (loại).
- Nếu NaOH phản ứng hết: 2b + c = 0,5 . 0,1 = 0,05 (III)
Từ (II) và (III) ta có : 106 b + 84(0,05 – 2b) = 2,96
62b = 1,24 suy ra: b= 0,02 và c = 0,01
Theo 2, 3 và 4, n co2 = 0,03= n MO = a = 0,03.
Thay giá trị a = 0,03 và (I) ta có: 0,07299M = 4,085
M = 56 vậy kim loại M là Fe, mMO=(56+16).0,03= 2,16 g
b/ Dung dịch E gồm FeSO4 0,03 mol và H2SO4 dư 0,02 mol. Khi cho Al phản ứng hoàn toàn tạo 1,12 gam chất rắn, H2SO4 phản ứng hết.
2Al+3H2SO4---->Al2(SO4)3+3H2
2Al+3FeSO4----->Al2(SO4)3+3Fe
Khối lượng Fe trong dung dịch E : 56 . 0,03 = 1,68 gam > 1,12 gam
Như vậy FeSO4 còn dư thì Al tan hết. Vây t = 1,12: 56 =0,02 mol
Vây n Al = 0,04 : 3 + 0,04:3 = (0,08 : 3) mol
Vây khối lượng x = 0,08: 3 . 27 = 0,72 gam

CaCO3+2HCl\(\rightarrow\)CaCl2+CO2+H2O
CaCO3+H2SO4\(\rightarrow\)CaSO4+CO2+H2O
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25mol\)
Gọi x, y lần lượt là số mol CaCl2 và CaSO4.Ta có hệ:
x+y=0,25
111x+136y=32,7
Giải ra x=0,052, y=0,198
Số mol HCl=x=0,052mol
\(C_{M_{HCl}}=\dfrac{0,052}{0,1}=0,52M\)
Số mol H2SO4=y=0,198mol
\(C_{M_{H_2SO_4}}=\dfrac{0,198}{0,1}=1,98M\)
\(m_{CaCO_3}=\left(0,052+0,198\right).100=25g\)

Ở 20oC: 100 gam nước hoà tan 32 gam KNO3
=> 500 gam nước hoà tan \(\frac{500.32}{100}=160\left(gam\right)KNO_3\)
Vậy khối lượng KNO3 tách ra khỏi dung dịch là:
450 - 160 = 290 (gam)
Gọi khối lượng KNO3 tách ra là a
Khối lượng của dung dịch ở 85°C là
mdd=mct+mH2O
=450+500=950(g)
mdd sau khi tách là
950-a(g)
mKNO3 có trong dung dịch sau khi tách là
450-a(g)
Ở 20°C 100 g H2O hòa tan 32 g KNO3 để tạo 132 g dung dịch bão hòa
Hay 100 g H2O hòa tan 450-a g KNO3 để tạo
950-a g dung dịch bão hòa
->32.(950-a)=132.(450-a)
->30400-32a=59400-132a
->132a-32a=59400-30400
->100a=29000
->a=290
Vậy khối lượng KNO3 tách ra là 290 g

Mg +H2SO4--->MgSO4 +H2
x x x x mol
Fe+ H2SO4---> FeSO4+ H2
y y y y mol
theo bài ta có : 24x+ 56y=1,36 và x+y=0,672/22,4
=> x=0,01 mol và y=0,02 mol
=> mMg=0,24 gam mFe=1,12 gam
tớ thấy đề bài khó để là ý b) bạn ạ nếu bạn xem lạ đề bài thì tốt quá![]()

Gọi hai kim loại cần tìm lần lượt là A(II) và B(III)
Gọi a,b lần lượt là số mol A, B
Đổi 170ml = 0,17l
A + 2HCl = ACl2 + H2 (1)
a 2a a a (mol)
2B + 6HCl = 2BCl3 + 3H2 (2)
b 3b b 1,5b (mol)
Số mol HCl là : 0,17 x 2= 0,34(mol) = 2a + 3b (mol)
Khối lượng HCl là: 0,34 x 36,5 = 12,41 (g)
Theo PTHH (1)(2): n H2 = a+1,5b= 1/2 nHCl= 0,34:2= 0,17 (mol)
Khối lượng H2 thu đc là: 0,17 x 2= 0,34(g)
Theo ĐL bảo toàn khối lượng:
mhh + m HCl = mMuối + m H2
=> m muối= 4 + 12,41 - 0,34 = 16,07(g)
b, Thể tích H2 thoát ra là: 0,17 x 22,4 = 3,808 (l)
c, Ta có: b= 5a
A + 2HCl = ACl2 + H2
a a (mol)
2Al + 6HCl = 2AlCl3 + 3H2
5a 7,5a (mol)
Số mol H2 thu được là: a+ 7,5a= 8,5a= 0,17(mol)
=> a= 0,02 (mol)
Ta có phương trình:
MA x a + 27 x 5a = 4 (g)
=> a ( MA + 135) =4 (g)
=> MA + 135 = 4/ 0,02= 200(g)
=> MA = 200 - 135= 65(g)
Vậy A là kim loại Zn