Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt nZn = x mol; nFe = y mol.
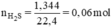
Ta có hệ phương trình: 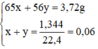
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g

Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)

a) Fe+H2SO4-->FeSO4+H2
Chất rắn X là Cu
Ta có
n H2=2,24/22,4=0,1(mol)
Theo pthh
n Fe=n H2=0,1(mol)
m Fe=0,1.56=5,6(g)
%m Fe=5,6/8,8.100%=66%
%m Cu=100-66=34%
b) Cu+2H2SO4--->CuSO4+SO2+2H2O
Ta có
m Cu=8,8-5,6=3,2(g)
n Cu=3,2/64=0,05(mol)
Theo pthh
n SO2=n Cu=0,05(mol)
V SO2=0,05.22,4=11,2(l)
Khác Dương
a)
Cho Fe và Cu vào H2SO4 loãng chỉ có Fe phản ứng.
Fe + H2SO4 \(\rightarrow\) FeSO4 + H2
Ta có: nH2=\(\frac{2,24}{22,4}\)=0,1 mol
\(\rightarrow\) nFe=nH2=0,1 mol
\(\rightarrow\) mFe=0,1.56=5,6 gam
\(\rightarrow\) mCu=8,8-5,6=3,2 gam\(\rightarrow\) nCu=0,05 mol
%Fe=\(\frac{5,6}{8,8}\)=63,6%\(\rightarrow\) %Cu=36,4%
b) 2Fe + 6H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3 SO2 + 6H2O
Cu + 2H2SO4 \(\rightarrow\) CuSO4 + SO2 + 2H2O
\(\rightarrow\) nSO2=\(\frac{3}{2}\)nFe + nCu=0,1.\(\frac{3}{2}\)+0,05=0,2 mol
\(\rightarrow\) VSO2=4,48 lít

Theo đề bài cho, bột S dư nên Fe và Zn tác dụng hết với S.
Phương trình hóa học của phản ứng:
Zn + S → ZnS
Fe + S → FeS
ZnS + H2SO4 → ZnSO4 + H2S
FeS + H2SO4 → H2S + FeSO4

Theo đề bài ta có bột S dư nên Fe, Zn tác dụng hết với S.
a)Phương trình hóa học của phản ứng.
Zn + S -> ZnS Fe + S -> FeS
x mol x mol y mol y mol
ZnSO4 + H2SO4 -> ZnSO4 + H2S
x mol x mol
FeSO4 + H2SO4 -> FeSO4 + H2S
x mol y mol
Ta có hệ phương trình :
Giải hệ phương trình => x = 0,04 (mol), y = 0,02 (mol).
Vậy mZn = 0,04.65 = 2,6g
mFe = 0,02.56 = 1,12g.

gọi số mol Cu, Al,Mg lần lượt là x,y,z
\(\left\{{}\begin{matrix}64x+27y+24z=8,3\\1,5y+z=\dfrac{5,6}{22,4}\\x=\dfrac{1,12}{22,4}\end{matrix}\right.\)=>\(\left\{{}\begin{matrix}x=0,05\\y=0,1\\z=0,1\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}\%nCu=20\%\\\%nAl=40\%\\\%nMg=40\%\end{matrix}\right.\)
gọi số mol Cu, Al,Mg lần lượt là x,y,z
⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩64x+27y+24z=8,31,5y+z=5,622,4x=1,1222,4{64x+27y+24z=8,31,5y+z=5,622,4x=1,1222,4=>⎧⎪⎨⎪⎩x=0,05y=0,1z=0,1{x=0,05y=0,1z=0,1
=>⎧⎪⎨⎪⎩%nCu=20%%nAl=40%%nMg=40%

a) Mg+H2SO4-->MgSO4+H2
Ta có
n H2=11,2/22,4=0,05(mol)
Theo pthh
n Mg=n H2=0,05(mol)
m Mg=0,05.24=1,2(g)
%m Mg=1,2/5,6.100%=21,43%
%m Cu=100-21,43=78,57%
b) Chất rắn sau pư là Cu = 5,6.1,2=4,4(g)
n Cu=4,4/64=0,06875(mol)
Cu+2H2SO4--->CuSO4+2H2O+SO2
Theo pthh
n SO2=n Cu=0,06875(mol)
V SO2=0,06875.22,4=1,54(l)
a)Hòa tan bằng H2SO4 thì chỉ có Mg tan
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2
Ta có: nH2=\(\frac{1,12}{22,4}\)=0,05 mol=nMg \(\rightarrow\)mMg=0,05.24=1,2 gam
\(\rightarrow\)mCu=5,6-1,2=4,4 gam \(\rightarrow\)nCu=\(\frac{4,4}{64}\)=0,06875 mol
Ta có: %Mg=\(\frac{1,2}{5,6}\)=21,4% \(\rightarrow\)%Cu=100%-%Mg=78,6%
b) Hòa tan bằng H2SO4 đặc nóng thì cả 2 kim loại đều tan hết
Quá trình cho e:
Mg\(\rightarrow\) Mg+2 +2e; Cu \(\rightarrow\)Cu+2 +2e
Quá trình nhận e: S+6 +2e \(\rightarrow\) S+4
Bảo toàn e:
2nMg + 2nCu=2nSO2
\(\rightarrow\) nSO2=nMg + nCu=0,05+0,06875=0,11875 mol
\(\rightarrow\) V SO2=0,11875.22,4=2,66 lít