Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nBr2=0,05 mol
SO2 + Br2 + H2O =>H2SO4 +2HBr
0,05 mol<=0,05 mol
Chỉ có Cu pứ vs H2SO4 đặc nguội
Cu =>Cu+2 +2e
0,05 mol<= 0,1 mol
S+6 +2e =>S+4
0,1 mol<=0,05 mol
=>nCu=0,05 mol=>mCu=3,2g
=>mAl=5,9-3,2=2,7g
=>nAl=0,1 mol
Tổng nhh cr=0,1+0,05=0,15 mol

nFe = 0,24 (mol)
*TH1: H2SO4 đặc còn dư sau phản ứng
2Fe + 6H2SO4 (đặc) -t\(^o\)-> Fe2(SO4)3 + 3SO2 + 6H2O (1)
0,24..............................................0,12
Theo (1) nFe2(SO4)3 = 0,12 (mol)
=> m muối = 0,12 . 400 = 48 (g) > 42,24 (g)
=> Loại
*TH2: H2SO4 tác dụng hết, Fe còn dư sau phản ứng với H2SO4.
Gọi a, b lần lượt là số mol của Fe pứ ở phương trình (2) và (3)
2Fe + 6H2SO4 (đặc) -t\(^o\)-> Fe2(SO4)3 + 3SO2 + 6H2O (2)
a..........3a...................................0,5a.............1,5a
Fe + Fe2(SO4)3 ---> 3FeSO4 (3)
b......................................3b
Ta có: a + b = 0,24 (I)
0,5a.400 + 3b.152 = 42,24 (II)
Từ (I) và (II) ta được: b < 0 (loai)
Chịu :V Chỉ là lúc đầu định hình ra cách giải, nhưng nghiệm thế này thì khó
Bài này ra 2 muối sắt cơ. Là FeSO4 và Fe2(SO4)3
Do H2SO4 đặc hết, Fe dư nên xẩy ra pứ
Fe + Fe2(SO4)3 \(\rightarrow\)3FeSO4

\(SO_2+Br_2+2H_2O--->H_2SO_4+2HBr\)
\(\Rightarrow\)SO2 làm nhạt màu dung dich nước brom
\(SO_2+2H_2S--->3S\downarrow+2H_2O\)
\(\Rightarrow\)Xuất hiện kết tủa vàng Lưu huỳnh (S).
\(CuO+H_2SO_4--->CuSO_4+H_2O\)
\(\Rightarrow\)Chất rắn màu đen Đồng (II) oxit CuO tan dần trong dung dịch.

Đáp án B
Cách 1: Viết phản ứng, cân bằng hệ số và tính toán theo yêu cầu:
Các phản ứng xảy ra như sau:
Do đó
Cách 2: Áp dụng phương pháp bảo toàn mol electron:
Ta có: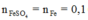 (bảo toàn nguyên tố Fe)
(bảo toàn nguyên tố Fe)