Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chất rắn m1 là Cu. Bảo toàn e có 2nCu=3nNO
→ 2b = 2V/70
Gọi số mol: Mg là x; Cu là y; Al là z và NH4NO3 là t
Ta có hệ phương trình
(1) 2x +3y = 2n(H2) = 0,88
(2) 24x + 64y + 27z = 19,92
(3) 148x + 188y + 213z + 80t = 97,95
(4) 2x + 2y + 3t = 3n(NO) + 8n(NH4NO3) = 3V/22,4 + 8t = 6,25y + 8t
→ x = 0,08; y = 0,18; z = 0,24
→ %Mg = 9,64% → Đáp án B

Đáp án : C
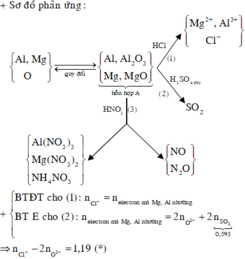
Bảo toàn e :
3nAl + 2nMg= 2 n S O 2 + 3 n N O + n N O 2 + 8 n N 2 O = 1,4 mol
Và 27nAl + 24nMg = 15g
=> nAl = 0,2 mol
=> %mAl = 36%

Định hướng tư duy giải
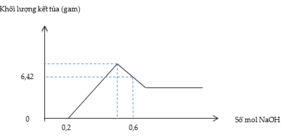
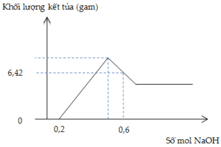
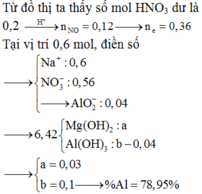
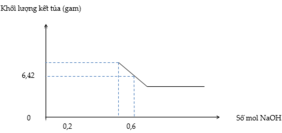
Từ đồ thị ta thấy số mol HNO3 dư là 0,2 → H + n N O = 0 , 12 → n e = 0 , 36
Tại vị trí 0,6 mol, điền số
→ N a + : 0 , 6 N O 3 - : 0 , 56 → A l O 2 - : 0 , 04 → 6 , 42 M g ( O H ) 2 : a A l ( O H ) 3 : b - 0 , 04 → a = 0 , 03 b = 0 , 1 → % A l = 78 , 95 %

Đáp án B
Do dung dịch Y tăng 21,28 gam.
→ m X = 28 , 96 - 21 , 28 = 7 , 68 g a m T a c ó : n X = 7 , 68 9 , 6 . 4 = 0 , 2 m o l
Do vậy ta giải được số mol CO2 và NO trong X lần lượt là 0,06 mol và 0,08 mol.
Vậy số mol FeCO3 là 0,06 mol.
Do khi thêm AgNO3 vào Y có xuất hiện NO nên H+ dư nên Y không có NO3- dư.
Bảo toàn N: n N H 4 + = 0 , 24 - 0 , 06 . 2 - 0 , 08 = 0 , 04 m o l
Gọi a, b lần lượt là số mol Mg, Fe3O4, c là số mol HCl.
Do vậy kết tủa chứa AgCl c mol và Ag.
→ 24 a + 232 b + 0 , 06 . 116 = 28 , 96
Do cho AgNO3 vào sinh ra 0,03 mol NO nên H+ dư 0,12 mol.
Bảo toàn e kết hợp bảo toàn điện tích:
c= 0,04+8b+0,06.2+0,08.3+0,06.8+0,04.8+0,12
Bảo toàn e:
n A g = 2 a + b + 0 , 06 - 0 , 04 . 8 - 0 , 08 . 3 - 0 , 03 . 3 - 0 , 06 . 8 = 2 a + b - 1 , 07 → 143 , 5 c + 108 ( 2 a + b - 1 , 07 ) = 238 . 58
Giải được: a=0,53; b=0,04; c=1,64.
%Mg= 43,92%
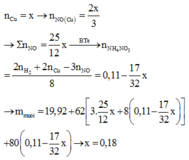
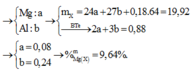


Đáp án C
Đặt số mol 2 kim loại lần lượt là a và b ta có:
+ PT theo khối lượng hh: 24a + 27b = 1,86 (1).
+ PT theo bảo toàn số mol e cho nhận: 2a + 3b = 8nN2O = 0,2 (2).
● Giải hệ (1) và (2) ta có nMg = a = 0,01 mol.
⇒ %mMg = 0 , 01 × 24 1 , 86 × 100 = 12,9%