Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Br2 + ddX → dẫn xuất halogen X. MX = 6,75.32 = 216 (đvC)
Từ khối lượng phân tử của dẫn xuất halogen ta có thể dùng phương pháp thử và suy ra công thức phân tử của dẫn xuất là C4H8Br2 đồng thời hiđrocacbon ban đầu là C4H8
Ứng với công thức này hợp chất có thể là anken hoặc xicloankan
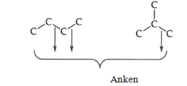
Xicloankan khi cộng Br2 thường sẽ ra nhiều hơn hai sản phẩm cộng
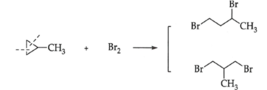
Đáp án B

Đáp án C
C nóng đỏ phản ứng với O2 thu được hỗn hợp khí có M=32
Þ 2 khí là CO và CO2 với tổng số mol bằng 0,04. Dùng quy tắc đường chéo được
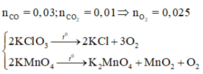
Gọi
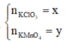
Có
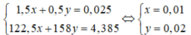
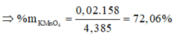

Đáp án C
C nóng đỏ phản ứng với O2 thu được hỗn hợp khí có M ¯ = 32
Þ 2 khí là CO và CO2 với tổng số mol bằng 0,04. Dùng quy tắc đường chéo được


\(M_X = 18.2 = 36(đvC)\)
X gồm CO2,CO
Ta có :
\(44n_{CO_2} + 28n_{CO} = 36(n_{CO_2} + n_{CO})\\ \Rightarrow 8n_{CO_2} = 8n_{CO}\\ \Rightarrow n_{CO_2} = n_{CO}\)
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH :
\(n_{CO} = n_{CO_2} = n_{CaCO_3} = \dfrac{20}{100} = 0,2(mol)\)
\(C + O_2 \xrightarrow{t^o} CO_2\\ 2C + O_2 \xrightarrow{t^o} 2CO\\ n_{O_2} = n_{CO_2} + \dfrac{n_{CO}}{2} = 0,3(mol)\\ \Rightarrow V = 0,3.22,4 = 6,72(lít)\)
\(\)

Chọn D
nHNO3 = 0,1 mol; nHCl = 0,5 mol
3Cu + 2HNO3 +6HCl → 3CuCl2 + 2NO +4H2O
→ HNO3 hết; nCu = 1,5. nHNO3 = 0,15 mol → mCu = 9,6g.

\(a,2KMnO_4+16HCl_{đặc}\rightarrow\left(t^o\right)2KCl+2MnCl_2+5Cl_2+8H_2O\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ Ta.có:n_{FeCl_3}=\dfrac{39}{162,5}=0,24\left(mol\right)\\ n_{Fe}=n_{FeCl_3}=0,24\left(mol\right)\\ n_{Cl_2}=\dfrac{3}{2}.0,24=0,36\left(mol\right)\\ n_{K_2MnO_4}=\dfrac{2}{5}.0,36=0,144\left(mol\right)\\ n_{HCl}=\dfrac{16}{5}.0.36=1,152\left(mol\right)\\ \Rightarrow a=m_{KMnO_4}=0,144.158=22,752\left(g\right)\\ b=C_{MddHCl}=\dfrac{1,152}{0,1}=11,52\left(M\right)\\ x=m_{Fe}=0,24.56=13,44\left(g\right)\\ V=V_{Cl_2\left(đktc\right)}=0,36.22,4=8,064\left(l\right) \)
\(b,n_{KCl}=n_{MnCl_2}=\dfrac{2}{5}.0,36=0,144\left(mol\right)\\ KCl+AgNO_3\rightarrow AgCl\downarrow\left(trắng\right)+KNO_3\\ MnCl_2+2AgNO_3\rightarrow2AgCl\downarrow\left(trắng\right)+Mn\left(NO_3\right)_2\\ n_{AgNO_3}=n_{AgCl}=n_{KCl}+2.n_{MnCl_2}=0,144+2.0,144=0,432\left(mol\right)\\ \Rightarrow m_{AgCl\downarrow\left(trắng\right)}=143,5.0,432=61,992\left(g\right)\\ m_{AgNO_3}=0,432.170=73,44\left(g\right)\\ \Rightarrow m_{ddAgNO_3}=\dfrac{73,44.100}{5}=1468,8\left(g\right)\)
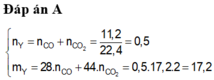
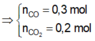
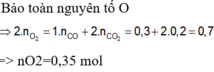
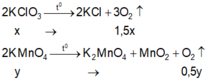
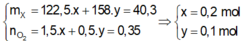
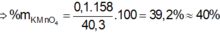



X có dạng CxHy
\(\%m_C=\frac{12x}{12x+y}=83,33\%=\frac{5}{6}\)
\(\Rightarrow72x=60x+5y\Rightarrow12x=5y\Rightarrow x:y=5:12\)
Vậy X có dạng (C5H12)n
Ta có:
\(2C+2\ge H\Rightarrow5n.2+2\ge12n\Rightarrow n=1\)
Vậy X là C5H12
X tác dụng với clo chỉ cho một dẫn xuất monoclo duy nhất
CTCT của X là : \(CH_3-C\left(CH_3\right)_2-CH_3\)
Tên gọi 2,2-dimetylpropan