Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bảo toàn Na: mol NaOH=2*mol Na2CO3 = 0.06
Bảo toàn khối lượng ==> mH2O = 2,76 + 40*0,06 - 4,44 = 0,72 ==> mol H2O = 0,04
CxHyOz + NaOH ---> muối CxHy-1O2Na + H2O (1)
----a--------0,06----------------------------------0,04
muối CxHy-1O2Na + O2 ----> CO2 + H2O + Na2CO3 (2)
------------------------------------0,11---0,05-----0,03
(1)+(2): CxHyO2Na + NaOH + O2 ----> CO2 + H2O + Na2CO3 (2)
-----------------a------------------------------0,11---0,09-----0,03
mol H: ay + 0,06 = 2*0.09 = 0,18 ===> ay = 0,12
Khi A cháy ==> mol H2O = 0,5ay = 0,06 ==> m H2O = 1,08
Theo bài ra, thu được 4,44g 2 muối + nước
\(\Rightarrow\) 2 x 76 + 0,06 x 40 = 4,44 + m(g) nước
A = CxHyO2
nC = 0,14mol; nH = 0,1 + 0,04 − 0,06 = 0,08
nO = \(\frac{2\times76-m_C-m_H}{16}\) = 0,06
\(\Rightarrow\) Công thức phân tử: C7H6O3.
Đốt cháy thu \(n_{H_2O}\) = 0,02 x 3 = 0,06 mol \(\Rightarrow\) \(m_{H_2O}\) = 0,06 x 18 = 1,08 gam.

Ta gọi nC=x ;nH=y ta được 12x+y=4,64
Ta có: m dd giảm=mkếttủa - (mCO2 + mH2O) => mCO2+mH2O
=mkettua- mdd giảm=39,4-19,912=19,488g
=> 44x+18.0,5y=10,688
Giải hpt: x=0,348; y=0,464 => x:y=3:4
=> CTĐGN của X là C3H4 => CTPT là C3H4.

Quy đổi hỗn hợp thành RCOOH
nRCOOH= 2nH2=0,5 mol => nOtrong axit=2nRCOOH=1 mol
m axit=mC+mH+mO=> mC=29,6-2.14,4/18-1.16=12 g => nCO2=nC=1 mol
CO2 + Ba(OH)2---> BaCO3+ H2O
nBa(OH)2=0,7 mol < nCO2 => Ba(OH)2 hết và CO2 dư
=> m Kết tủa = 0,7*(MBaCO3)=137,9 gam.
nCOOH= nNaHCO3=nCO2=0,5 mol => nOtrong axit=2nCOOH=1 mol
m axit=mC+mH+mO=> mC=29,6-2.14,4/18-1.16=12 g => nCO2=nC=1 => mCO2=44

MA = 44,5 . 2 = 89 (g/mol)
Ta có: mC = = 3,6 (gam); mH =
= 0,7 (gam)
mN = = 1,4 (gam); mO = 8,9 – (3,6 + 0,7 + 1,4) = 3,2 (gam)
Gọi CTPT của A là CxHyOzNt,
x : y : z : t = = 0,3 : 0,7 : 0,2 : 0,1 = 3 : 7 : 2 : 1
=> CTPT của A là (C3H7O2N)n ; MA = 89 g/mol => n = 1
Vậy CTPT của A là C3H7O2N
CTCT: 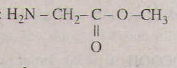
![]()
MA= 44,5.2=89
=> nX= 8,9/89=0,1 mol
Đặt CTTQ của X là CxHyNzO1 ( 0,1 mol)
CxHyNzO1 + (x+y/4 - z/2)O2----> xCO2 + y/2H2O + t/2N2
0,1----> 0,1.(x+y/4 - z/2)-----> 0,1x----->0,05y---->0,05t
Ta có:
0,1x=13,2/44
0,05y=6,3/18
0,05t=1,12/22,4
12x+y+16z+14t=89
HỎI:
Tại sao lại ra kết quả này: 12x+y+16z+14t
Lấy 12 và y và 16 và 14 ở đâu ra vậy?
Hay:
có phải nó là cái bắt buộc, bài nào nào tưong tự như vậy cũng phải có:12x+y+16z+14t

C4H7OH(COOH)2 + 2NaOH---> C4H7OH(COONa)2 + 2H2O)
C4H7OH(COONa)2+ 2HCl ----> C4H7OH(COOH)2+ 2NaCl
C4H7OH(COOH)2 + 3Na----> C4H7ONa(COONa)2+ 3/2 H2
0,1 0,15 mol
=> nH2= 0,15 mol
Từ các phản ứng trên ta suy ra X là anhiđrit có công thức là (HO − CH2 − CH2−CO)2O
Từ đó suy ra Z là acid có công thức : HOCH2CH2COOH
Khi lấy 0,1 mol Z tác dụng với NaOH thì ta thu được 0,1 mol H2.
Chọn B

Gọi công thức của Oxit Sắt là : \(Fe_xO_y\)
Các PTHH khi X vào HCl :
\(Fe+2HCl\rightarrow FeCl_2+H_2\)(1)
\(Fe_xO_y+2yHCl\rightarrow FeCl_{\frac{2y}{x}}+yH_2O\) (2)
nHCl ban đầu =\(\frac{200.14,6}{100.36,5}=0.8\left(mol\right)\)
\(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\Rightarrow m_{H_2}=0,1.2=0,2\left(g\right)\)
Từ (1) \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Fe_xO_y}=17,2-5,6=11,6\left(g\right)\Rightarrow n_{Fe_xO_y}=\frac{11,6}{56x+16y}\left(mol\right)\left(3\right)\) Từ (1) \(n_{HCl}=2n_{H_2}=2.0,1=0,2\left(mol\right)\)
\(m_{ddA}=200+17,2-0,2=217\left(g\right)\)
\(m_{ddB}=217+33=250\left(g\right)\)
\(n_{HCldu}=\frac{250.2,92}{100.36,5}=0,2\left(mol\right)\)
\(n_{HCl\left(2\right)}=0,8-0,2-0,2=0,4\left(mol\right)\)
\(n_{Fe_xO_y}=\frac{1}{2y}n_{HCl}=\frac{1}{2y}.0,4=\frac{0,2}{y}\left(mol\right)\)(4)
Từ (3) và (4) ta có pt :\(\frac{11,6}{56x+16y}=\frac{0,2}{y}\Rightarrow\frac{x}{y}=\frac{3}{4}\)
Vậy CT Oxit cần tìm là :Fe3O4
