Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\n_{NaOH}=\dfrac{164\cdot1,22\cdot20\%}{40}=1,0004\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo muối trung hòa
PTHH: \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Vì NaOH dư nên tính theo CO2 \(\Rightarrow\left\{{}\begin{matrix}n_{Na_2CO_3}=0,25\left(mol\right)\\n_{NaOH\left(dư\right)}=0,5004\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Na_2CO_3\left(rắn\right)}=0,25\cdot106=26,5\left(g\right)\\m_{NaOH\left(rắn\right)}=0,5004\cdot40=20,016\left(g\right)\end{matrix}\right.\)
*Các bài còn lại bạn làm theo gợi ý bên dưới
PTHH: \(CO_2+NaOH\rightarrow NaHCO_3\) (1)
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\) (2)

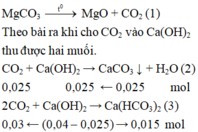
C a H C O 3 2 + 2 N a O H d ư → C a C O 3 ↓ + N a 2 C O 3 + 2 H 2 O ( 4 ) 0 , 015 → 0 , 015 m o l
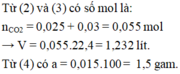
Đáp án A

a)
Gọi $n_{Na_2CO_3} = a(mol) ; n_{NaHCO_3} =b (mol)$
$2NaOH + CO_2 \to Na_2CO_3 + H_2O$
$NaOH +C O_2 \to NaHCO_3$
Ta có :
$106a + 84b = 13,7$
$2a + b = 0,2$
Suy ra: a = 0,05 ; b = 0,1
$n_{CO_2} = a + b = 0,15(mol)$
$V = 0,15.22,4 = 3,36(lít)$
b)
$Ca(OH)_2 + Na_2CO_3 \to CaCO_3 + 2NaOH$
$n_{CaCO_3} = a = 0,05(mol)$
$m = 0,05.100 = 5(gam)$
c)
$n_{Na_2CO_3} = a + 0,5b = 0,1(mol)$
$a = 0,1.106 = 10,6(gam)$

Chọn B
Cho hỗn hợp chất rắn phản ứng với HCl dư có Cu không phản ứng.
Phương trình hóa học:
F e + 2 H C l → F e C l 2 + H 2 F e O + 2 H C l → F e C l 2 + H 2 O


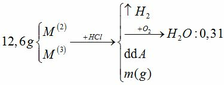
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
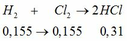

nCO2= 2,24/22,4= 0,1mol
nNaOH= 0,5.0,3=0,15mol
xét tỉ lệ T=nNaOH/nCO2 = 0,15/0,1= 1,5
=> phản ứng sinh ra 2 muối Na2CO3 và NaHCO3
CO2+ 2NaOH -> Na2CO3 + H2O
a 2a a (mol)
CO2+ NaOH-> NaHCO3
b b b (mol)
ta có hệ phương trình : a+b=0,1 (1)
2a+b=0,15 (2)
từ (1)và (2) => a=b=0,05
m= mNa2CO3+mNaHCO3 = 106.0,05 + 84.0,05 =9,5(g)