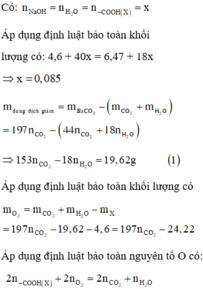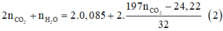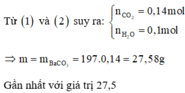Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi công thức TB của hai muối cacbonat là: M ¯ C O 3
M ¯ C O 3 → t 0 M O + C O 2 ( 1 )
Chất rắn Y ( M ¯ C O 3 ; M ¯ O )
n C O 2 ( 1 ) = 3 , 36 22 , 4 = 0 , 15 m o l
Y tác dụng với dung dịch HCl dư
M ¯ C O 3 + 2 H C l → t 0 M ¯ C l 2 + C O 2 + H 2 O ( 2 ) M ¯ O + H C l → t 0 M ¯ C l 2 + H 2 O ( 3 ) C O 2 + B a ( O H ) 2 → B a C O 3 + H 2 O ( 4 ) 2 C O 2 + B a ( O H ) 2 → B a ( H C O 3 ) 2 ( 5 ) B a ( H C O 3 ) 2 → t 0 B a C O 3 + C O 2 + H 2 O ( 6 ) n B a C O 3 ( 4 ) = 9 , 85 197 = 0 , 05 m o l n B a C O 3 ( 6 ) = 9 , 85 197 = 0 , 05 m o l
Theo PT (4,5,6): n C O 2 ( 3 ) = 0 , 15 m o l
Theo PT (1,2):
n M ¯ C O 3 = n C O 2 ( 2 ) + n C O 2 ( 1 ) = 0 , 15 + 0 , 15 = 0 , 3 m o l
Muối khan là: M ¯ C l 2
M ¯ C O 3 → M ¯ C l 2 M ¯ + 60 M ¯ + 71
0,3 mol muối cacbonat pư tạo 0,3 mol muối clorua tăng 3,3(g).
Khối lượng muối cacbonat ban đầu là: 38.15-3,3= 34,85(g)
Giá trị của m = 34,85(g)

Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3 → MO + CO2
n C O 2 = 3,36 /22,4 = 0,15 mol → n M C O 3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
n C a C O 3 = 15/100 = 0,15 mol
→ n M C O 3 dư = 0,15 mol
n M C O 3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có:
n M C O 3 = n M C l 2 = 0,3 (mol)
Bảo toàn khối lượng có:
m M C O 3 = m M C l 2 - 0,3.(71- 60) = 29,2 (gam)

Đáp án C
Gọi số mol mỗi ion NH4+, K+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = 0,3 mol
mkết tủa= mBaCO3+ mBaSO4= 197z+233t= 43 suy ra t= 0,1 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol= 0,1
Định luật bảo toàn điện tích: x+y=2z+ 2t suy ra y= 0,1 mol
mmuối= (18x+ 39y+60z+96t).2= 49,8 gam

Lời giải
n C O 2 sin h r a t r o n g p h ả n ứ n g c ộ n g N a H C O 3 = n C O O H = 0 , 4 ( m o l ) ⇒ n N a t r o n g m u ố i = 0 , 4 ( m o l )
Khi đốt cháy T thu được Na2CO3; CO2 và H2O trong đó ta có:
n C O 2 = n C a C O 3 = 0 , 2 ( m o l ) .
Bảo toàn nguyên tố Na
n N a 2 C O 3 = 1 2 n N a t r o n g m u ố i = 0 , 2 ( m o l )
Bảo toàn nguyên tố C
⇒ n C t r o n g a x i t = n C O 2 ( c h , y ) + n N a 2 C O 3 = 0 , 4 ( m o l )
Đến đây, quan sát các đáp án ta xét 3 trường hợp:
Trường hợp 1: Nếu cả 2 axit đều đơn chức
⇒ n a x i t = n C O O H = 0 , 4 ( m o l ) ⇒ C ¯ a x i t = 1
=>không thỏa mãn
Trường hợp 2: Nếu cả 2 axit đều 2 chức
⇒ n a x i t = n C O O H 2 = 0 , 2 ( m o l ) ⇒ C ¯ a x i t = 2
.Mà cả 2 axit đều 2 chức =>không thỏa mãn
Trường hợp 3: Một axit đơn chức và một axit 2 chức
⇒ n C O O H 2 < n a x i t < n C O O H ⇒ 0 ,...

Lời giải
n C O 2 = 0 , 4 ( m o l ) ⇒ n - C O O H = n - C O O N a = 0 , 4 ( m o l )
Đốt cháy muối khan ta thu được Na2CO3; CO2 và H2O.
Ta có n N a 2 C O 3 = 1 2 n H C O O N a = 0 , 2 ( m o l ) ; n C O 2 = 0 , 2 ( m o l )
Bảo toàn nguyên tố C n C t r o n g X = 0 , 4 ( m o l ) = n - C O O H
=> 2 axit chỉ có thể là HCOOH và (COOH)2
Đáp án A.