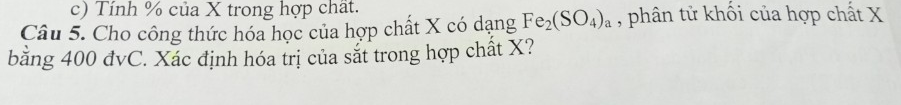Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Sai:
CaOH -> Ca (OH)2
Na2PO4 -> Na3PO4
H3S -> H2S
NaO -> Na2O
H2NO2 -> HNO2
Còn lại là đúng rồi bạn

a/\(H_2+FeO\rightarrow^{t^0}Fe+H_2O\) . Phản ứng oxi hóa-khử.
b/\(4Na+O_2\rightarrow^{t^0}2Na_2O\). Phản ứng hóa hợp
c)\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\). Phản ứng thế
d)\(2KClO_3\rightarrow^{t^0}2KCl+3O_2\uparrow\). Phản ứng phân hủy
\(H_2+FeO\rightarrow\left(t^o\right)Fe+H_2O\) : pứ oxi hóa-khử, pứ thế
\(4Na+O_2\rightarrow\left(t^o\right)2Na_2O\) : pứ hóa hợp
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) : pứ thế
\(KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\) : pứ phân hủy

\(M_{SO_{2}}\)=32+16.2=64g/mol
\(M_{O_{2}}\)=16.2=32 g/mol
\(d_{M_{SO_{2}}/{M_{O_{2}}}}\)= \(\dfrac{M_{SO_{2}}}{M_{O_{2}}}\)=\(\dfrac{64}{32}\)=2
Vậy SO2 nặng hơn O2 2 lần

a, 3Fe + 2O2 => Fe3O4 : phản ứng hoá hợp ( nhiệt độ )
| b, Mg + O2 => MgO : phản ứng hoá hợp ( nhiệt độ ) | |
| c, 2KMnO4 => K2MnO4 + MnO2 + O2 : phản ứng phân huỷ ( nhiệt độ ) | |
| d, 2H2O => 2H2 + O2 : phản ứng phân huỷ ( điện phân bằng dòng điện 1 chiều) | |
| e, Na2O + H2O => 2NaOH : phản ứng hoá hợp | |
| f, P2O5 + 3H2O => 2H3PO4 : phản ứng hoá hợp | |
+ O2 => Fe3O4: phản ứng hoá hợp

\(PTK_x=2\cdot56+\left(32+16\cdot4\right)a=400\\ \Rightarrow96a=288\\ \Rightarrow a=3\)
Do đó CTHH \(X:Fe_2\left(SO_4\right)_3\)
Vì \(SO_4\left(II\right)\Rightarrow Fe\left(III\right)\)


Gọi CTHH là \(S_xO_y\)
ta có M S : M O = \(\dfrac{32x}{16y}=\dfrac{2}{3}\)
=> \(\dfrac{x}{y}=\dfrac{1}{3}\)
vậy CTHH là \(SO_3\)

4Al+3O2-to>2Al2O3
0,1----0,075---0,05 mol
n Al=0,1 mol
=>m Al2O3=0,05.102=5,1g
`=>` Ta có:
`4Al + 3O2 -to> 2Al_2O3
`0,1----0,075---0,05` `mol`
`n` `Al` `= 0,1` mol`
=> m Al_2O3 = 0,05 . 102 =5,1g`