Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)\(n_{Fe_2O_3}=0,1mol;n_{CuO}=0,08mol;n_{H_2SO_4}=0,32mol\)
Xét trường hợp 1: \(Fe_2O_3\) phản ứng trước, Ta có phản ứng
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,1 0,3 0,1 0,3 (mol)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
0,02 0,02 0,02 0,02 (mol)
\(\Rightarrow m=m_{CuOdư}=80\cdot\left(0,08-0,02\right)=4,8g\)
Trường hợp 2: CuO phản ứng trước, Ta có phản ứng
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
0,08 0,08 0,08 0,08 (mol)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,08 0,24 0,08 0,24 (mol)
\(\Rightarrow m=m_{Fe_2O_3dư}=160\cdot\left(0,1-0,08\right)=3,2g\)
Vậy giá trị của m nằm trong khoảng biến thiên 3,2g<m<4,8g

TH1:
\(Fe+2HCl\rightarrow FeCl_2+H_2\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(m_{Cu}=m_{rắn}=6,4\left(g\right)\\ \Rightarrow m_{\left(Fe,Fe_2O_3\right)}=28-6,4=21,6\left(g\right)\\ n_{FeCl_2}=n_{Fe}=n_{H_2}=0,15\left(mol\right)\\ \Rightarrow n_{Fe_2O_3}=\dfrac{21,6-0,15.56}{160}=0,0825\left(mol\right)\\ \Rightarrow n_{FeCl_3}=2.0,0825=0,165\left(mol\right)\\ \Rightarrow m_{muối}=m_{FeCl_2}+m_{FeCl_3}=127.0,15+162,5.0,165=45,8625\left(g\right)\)
TH2: Nếu cho 28 gam hỗn hợp đó tác dụng clo thì như nào nhở???

NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%

Cu ko td vs HCl.
Zn+2HCl=ZnCl2+H2
nH2=o.2 mol =nZn
mZn=0.2×65=13g
mCu=20-13=7g.
nHCl=2nH2=0.4mol.
VHCl=n\CM =0.8l

\(n_{HCl}=\dfrac{292.15\%}{36,5}=1,2\left(mol\right)\)
\(n_{Al_2O_3}=\dfrac{24,48}{102}=0,24\left(mol\right)\)
PTHH: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
Xét tỉ lệ: \(\dfrac{0,24}{1}>\dfrac{1,2}{6}\) => Al2O3 dư, HCl hết
PTHH: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
0,2<--1,2
=> \(\left\{{}\begin{matrix}m_{Cu}=0,35.64=22,4\left(g\right)\\m_{Al_2O_3}=\left(0,24-0,2\right).102=4,08\left(g\right)\end{matrix}\right.\)
=> mrắn = 22,4 + 4,08 = 26,48 (g)
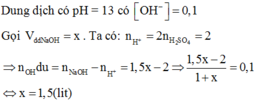
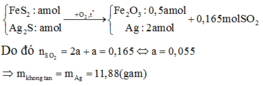
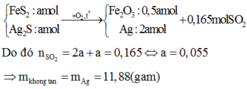

Vì đây là hh 2 oxit nên khi cho HCl vào thì 2 oxit đều pư nên ko biết oxit nào pư trước
nCuO=6.4/80=0.08
nFe2O3=16/160=0.1
nHCl=0.64
TH1 giả sử CuO pư trước
CuO+2HCl--->CuCl2+H2O (1)
0.08:>0.16
nHCl còn lại = 0.48
Fe2O3+6HCl--->2FeCl3+3H2O (6)
0.08<:::::0.48
vì 0.08<0.1=>nFe2O3 dư =0.02 mol
=> mFe2O3 dư=0.02*160=3.2g
TH2 giả sử Fe2O3 pư trước
theo (2)nHCl pư = 6nFe2O3=0.6
=> nHCl còn lại = 0.04
theo (1) nCuO=0.5nHCl còn lại = 0.02
mà 0.02<0.08=> CuO dư 0.06 mol
mCuO dư = 0.06*80=4.8g
nhưng trong thực tế 2 oxit tan đồng thời nên m chất rắn không tan biến thiên trong khoảng 3.2<m<4.8
Nguồn: Sưu tầm