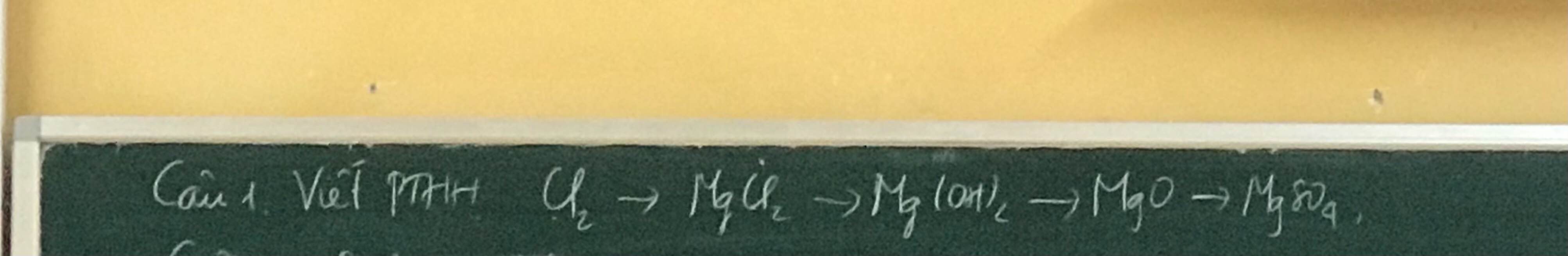Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Anh nhớ em đăng 1 lần nhưng câu 1 câu 2 anh chả thấy có đánh số để chọn
Anh nhắm theo mắt anh nhé
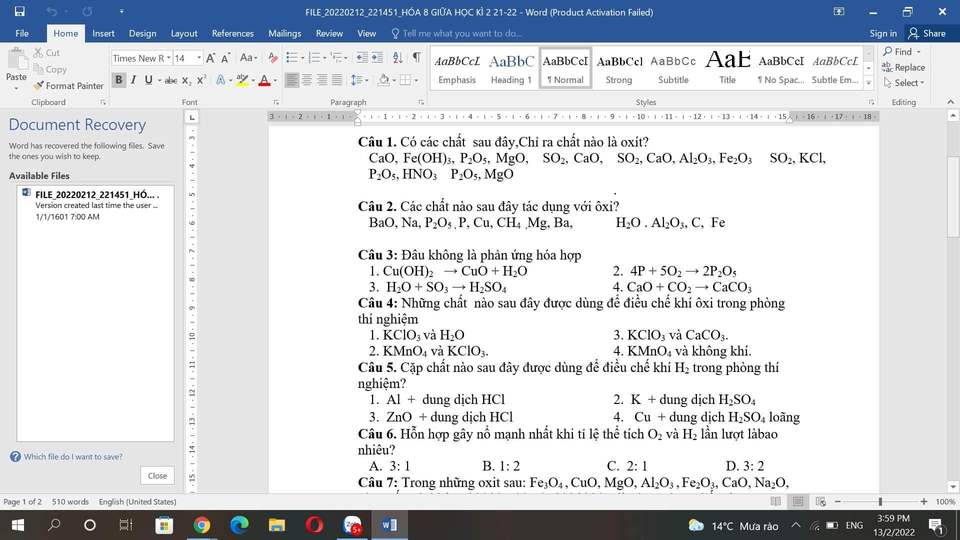
Câu 1: Chọn nhóm SO2, CaO, Al2O3, Fe2O3
Câu 2: Na, P, Cu, CH4, Mg, Fe, C, Ba
Câu 3: 1
Câu 4: 2
Câu 5: 1
Câu 6: B


a) \(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1125->0,3375
=> \(V_{H_2}=0,3375.22,4=7,56\left(l\right)\)
b) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1125}{1}>\dfrac{0,2}{3}\) => H2 hết, Fe2O3 dư
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,2-------->\(\dfrac{0,4}{3}\)
=> \(m_{Fe}=\dfrac{0,4}{3}.56=\dfrac{112}{15}\left(g\right)\)

\(Cl_2+Mg-^{t^o}\rightarrow MgCl_2\\ MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\\ Mg\left(OH\right)_2-^{t^o}\rightarrow MgO+H_2O\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)

Gọi x,y là số mol của Al , Mg
a.2Al + 3H2SO4 ----> Al2(SO4)3 + 3H2
x _______________________ 3/2x
4Mg + 5H2SO4 ---> 4MgSO4 + H2
y______________________ 1/4y
b. Số mol của H2 là
\(^nh2=\)\(\dfrac{V}{22,4}\) = \(\dfrac{8,96}{22,4}\) = 0,4 (mol)
\(\dfrac{3}{2}\)x + \(\dfrac{1}{4}\)y = 0,4 ⇒ x = 0,195
27x + 24y =15,6 y= 0,43
\(^mAl=\) 0,195 . 27 = 5,265 (g)
\(^mMg=\) 0,43 . 24 = 10,32 (g)
%\(^mAl\) = \(\dfrac{5,256.100\%}{15,6}\)= 33,.75%
\(^{\%m}Mg=\)100% - 33,75% = 66,25%

\(4Na+O_2\rightarrow2Na_2O\)
\(Ca+\dfrac{1}{2}O_2\rightarrow CaO\)
\(S+O_2\xrightarrow[]{t^o}SO_2\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\uparrow\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(H_2+\dfrac{1}{2}O_2\xrightarrow[]{t^o}H_2O\)
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
\(H_2+PbO\xrightarrow[]{t^o}Pb+H_2O\)

Thả vào nước và cho thử quỳ tím:
- Quỳ tím chuyển xanh -> BaO
- Quỳ tím chuyển đỏ -> P2O5
- Quỳ tím ko đổi màu -> CaCO3

a.\(C\%_{KCl}=\dfrac{20}{600}.100=3,33\%\)
b.2,5kg = 2500g
\(C\%_{Al_2\left(SO_4\right)_3}=\dfrac{34,2}{2500}.100=1,368\%\)