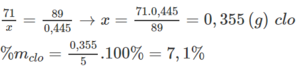Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2Fe+3Cl_2\rightarrow2FeCl_3\)
\(2Al+3Cl_2\rightarrow2AlCl_3\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
\(n_{Fe\left(OH\right)3}=\frac{2,14}{107}=0,02\left(mol\right)\)
\(\Rightarrow n_{Fe}=0,02\left(mol\right)\)
\(m_{Fe}=0,02.56=1,12\left(g\right)\)
\(m_{Al}=1,39-1,12=0,27\left(g\right)\)
\(n_{Al}=\frac{2,7}{27}=0,1\left(mol\right)\)
\(\Rightarrow n_{Cl2}=0,02.1,5+0,01.1,5=0,045\left(mol\right)\)
\(\Rightarrow V_{Cl2}=0,45.22,4=10,08\left(l\right)\)
\(m=m_{AlCl3}+m_{FeCl3}=4,585\left(g\right)\)

1.
TH1: Không có muối của Flo \(\Rightarrow\) Tạo 2 kết tủa
\(NaB+AgNO_3\rightarrow NaNO_3+AgB\)
0,03______0,03______0,03__________
\(n_{AgNO_3}=0,15.0,2=0,03\left(mol\right)\)
\(\Rightarrow m_{NaB}=0,03.\left(23+M_B\right)=2,2\)
\(\Rightarrow M_B=50,33\)
\(\Rightarrow M_X< 50,33< M_Y\)
Vì X, Y thuộc 2 chu kỳ liên tiếp nên X, Y lần lượt là: Cl và Br
\(m_{NaNO3}=0,03.85=2,55\left(g\right)\)
Theo ĐLBTKL, ta có:
mAgB = ( mNaB + mAgNO3 ) - mNaNO3
\(=\left(2,2+5,1\right)-2,55=4,75\left(g\right)\)
TH2: Có muối của flo \(\Rightarrow\) Có 1 kết tủa là AgCl
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\)
\(n_{AgCl}=n_{AgNO3}=0,03\left(mol\right)\)
\(\Rightarrow m_{AgCl}=0,03.143,5=4,305\left(g\right)\)

gọi số mol của hỗn hợp muối là \(\begin{cases}X_2CO_3:2x\\XHCO_3:2y_{ }\\XCl:2z\end{cases}\)
gọi số mol HCl : a mol
ptpu : X2CO3 + 2HCl = 2XCl + CO2 + H2O
XHCO3 + HCl = XCl + CO2 + H2O
khí B : CO2 có số mol = 0,4 mol = 2x + 2y (1)
dd A gồm : \(\begin{cases}XCl:2\left(2x+y+z\right)\\HCl_{dư}=a-4x-2y\end{cases}\)
Phần 1 : hh A + AgCl = kết tủa
kết tủa ở đây chính là AgCl => số mol AgCl = 0,48 mol
=> z + \(\frac{a}{2}\)=0,48 => a = (0,48 -z) / 2 (2)
Phần 2 : nKOH = 0,1 = \(\frac{1}{2}\)nHCl dư => a -4x -2y = 0,2 (3)
hốn hợp muối gồm : \(\begin{cases}XCl:2x+y+z\\KCl:0,1\end{cases}\)
m hỗn hợp muối = 29,68 = (2x + y+z) .(X+35,5) = 29,68 -39.0,1 = 22,23 (4)
từ (2) thay vào (3) => (2x + y +z) = 0,38 (5)
từ (5) thay vào (4) ta tìm được X = 23 => X là Na
Đến đây bạn tự giải câu b nhé

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ PTHH:2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Fe+2HCl\rightarrow FeCl_2+3H_2\\ Đặt:n_{Al}=a\left(mol\right);n_{Fe}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}27a+56b=11\\1,5a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ a,n_{HCl}=2.n_{H_2}=2.0,4=0,8\left(mol\right)\\ \Rightarrow V_{ddHCl}=\dfrac{0,8}{8}=0,1\left(l\right)\\ b,FeCl_2+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2AgCl\downarrow\\ AlCl_3+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3AgCl\downarrow\\ n_{AgCl}=n_{AgNO_3}=3.n_{AlCl_3}+2.n_{FeCl_2}=3.a+2.b=3.0,2+2.0,1=0,8\left(mol\right)\\ \Rightarrow a=\dfrac{170.0,8}{250}.100=54,4\%\\ b=m_{\downarrow}=m_{AgCl}=0,8.143,5=114,8\left(g\right)\)

a. Cho brom vào thì có phản ứng với NaI
2NaI + Br2 → 2NaBr + I2 (1)
Gọi x, y lần lượt là số mol NaBr, NaI ban đầu
Khối lượng giảm là Δm = m_NaI – m_NaBr (1) = 150y – 103y = 47y = a (i)
Sau phản ứng số mol NaBr trong B là n_NaBr (2) = x + y
Cho Clo vào dd B thì NaBr phản ứng với clo
2NaBr + Cl2 → 2NaCl + Br2 (2)
Khối lượng muối giảm là Δm = m_NaBr (2) – m_NaCl (2) = 103(x + y) – 58,5(x + y) = 44,5(x + y) = a (ii)
Từ (i) và (ii) suy ra 47y = 44,5(x + y)
<=> 2,5y = 44,5x
<=> y = 17,8x
m_NaBr = 103x
m_NaI = 150y = 2670x
m_A = 2773x
%m_NaBr = 103/2773 = 3,71%
%m_NaI = 100% – 3,71% = 96,29%
Gọi x,y là số mol của NaI , NaBr
\(Br_2+2NaI\rightarrow2NaBr+I_2\)
0,5x____x_______x_____0,5x
\(\Rightarrow m_{muoi.giam}=m_{I2}-m_{Br2}\)
\(=127x-80y=47x\left(g\right)\)
\(Cl_2+2NaBr\rightarrow2NaCl+Br_2\)
0,5(x+y)__x+y_________0,5(x+y)
\(\Rightarrow m_{muoi.giam}=m_{Br2}-m_{Cl2}\)
\(=80\left(x+y\right)-35,5\left(x+y\right)\)
\(=44,5x+44,5y\left(g\right)\)
\(\Rightarrow44,5x+44,5y=47x\)
\(\Rightarrow2,5x=44,5y\Leftrightarrow\frac{x}{y}=\frac{44,5}{2,5}=\frac{89}{5}\)
Nếu \(n_{NaI}=98\left(mol\right)\)\(\Rightarrow n_{NaBr}=5\left(mol\right)\)
\(\%_{NaI}=\frac{89.150.100}{89.150+103.5}=96,29\%\)
\(\%_{NaBr}=100\%-96,29\%=3,71\%\)

Khi cho 5g Br 2 có lẫn Cl 2 phản ứng với KBr thì khối lượng muối giảm là :
1,600 - 1,155 = 0,445 (g)
Cl 2 + 2KBr → 2KCl + Br 2
Lý thuyết: 71 g 238 g 149 g khối lượng muối giảm đi 238 – 149 = 89 g
Thực tế: x g 0,445 g khối lượng muối giảm
Ta có: