
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



8) ta có PTHH chữ:
cacbon + khí oxi ➜ cacbon oxit
theo ĐLBTKL ta có
mC + mO2 = mCO2
=> mO2 = mCO2 - mC
thay số mO2 = 22 - 6 = 16 (g)
vậy cần 16g khí oxi :333

Bài 11:
a) Số mol phân tử khí O2:
\(n_{O2}=\dfrac{3,01.10^{24}}{6,02.10^{23}}=5\left(mol\right)\)
b) Khối lượng khí O2 là:
\(m_{O2}=32.5=160\left(g\right)\)
c) Thể tích khí O2 ở đktc:
\(V_{O2\left(đktc\right)}=5.22,4=112\left(l\right)\)
Bài 9:
nO2= 48/32=1,5(mol)
a) PTHH: C + O2 -to-> CO2
Ta có: nC=nCO2=nO2=1,5(mol)
=>mC=1,5.12=18(g)
b) PTHH: S+ O2 -to-> SO2
Ta có: nS= nSO2=nO2= 1,5(mol)
=>mS=1,5.32=48(g)
c) PTHH: 4 P + 5 O2 -to-> 2 P2O5
Ta có: nP= 4/5. nO2= 4/5. 1,5=1,2(mol)
=>mP= 1,2.31=37,2(g)


Ta có:
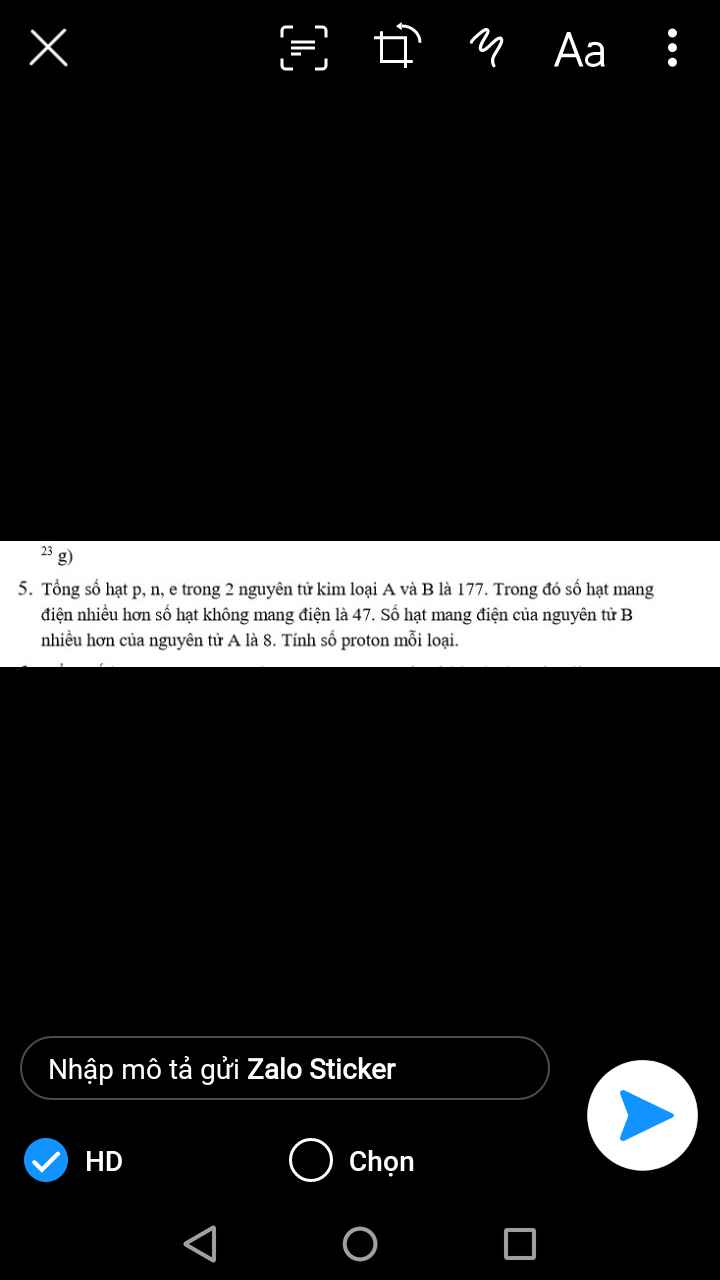
\(2p_A+n_A+2p_B+n_B=117\)
\(\left(2p_A+2p_B\right)-\left(n_A+n_B\right)=47\)
⇒\(2p_A+2p_B=112\left(1\right);n_A+n_B=65\)
Hạt mang điện của B nhiều hơn hạt mang điện của A là 8 :
\(2p_B-2p_A=8\left(2\right)\)
Từ (1) và (2):
⇒\(p_A=26\left(Fe\right);p_B=30\left(Zn\right)\)
Vậy số proton của A là 26 ; số proton của B là 30

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{Cu}=\dfrac{40}{80}=0,5\left(mol\right)\)
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\left(1\right)\)
Xét tỉ lệ: \(\dfrac{0,5}{1}>\dfrac{0,1}{1}\) => CuO dư, tính theo H2
Theo PT \(\left(1\right):n_{Cu}=n_{H_2}=0,1\left(mol\right)\)
\(\rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)




 mn giúp mik bài 9 vs bài 11 nha mik đg cần gấp
mn giúp mik bài 9 vs bài 11 nha mik đg cần gấp

đây là toán hay hoá vậy
hóa đó mình gặp roài đề thi quốc gia hóa 2020 khó lém : )