
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khi đun nóng, phản ứng thủy phân diễn ra tạo NaOH làm hoa hồng chỉ thị phenolphthalein. Phản ứng chuyển dịch theo chiều thuận.

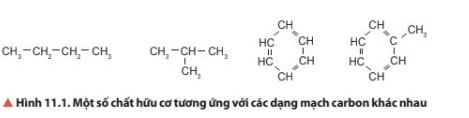
Từ trái sang phải: Thẳng, nhánh, vòng, vòng có nhánh

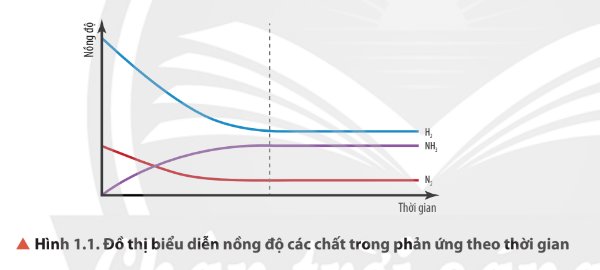
\(\left[N_2\right],\left[H_2\right]\) giảm, \(\left[NH_3\right]\) tăng.
Sau mốc thời gian nhất định, nồng độ các chất không thay đổi.

- Bước 2: để yên một thời gian, hỗn hợp trong phễu tách lớp. Tinh dầu quýt tan trong hexane, nước không ta trong hexane, do đó sau một thời gian sẽ có hiện tượng tách lớp: một lớp nước nặng hơn ở dưới và một lớp gồm hỗn hợp hexane, tinh dầu quýt nhẹ hơn ở trên.
- Bước 3: vặn khoá phễu từ từ, lớp nước phía dưới chảy vào bình tam giác, lớp trên là hỗn hợp hexane và tinh dầu quýt được lấy ra khỏi phễu bằng
- Bước 4: Làm bay hơi hexane để thu được tinh dầu quýt. Hexane có nhiệt độ sôi thấp hơn tinh dầu quýt, do đó khi làm bay hơi hỗn hợp, hexane bay hơi trước, còn lại tinh dầu quýt.

CH3COONa(aq) + H2O(l) ⇌ CH3COOH(aq) + NaOH(aq)
Hiện tượng: Khi đun nhẹ bình (1), dung dịch trong bình (1) hóa hồng.
Nhận xét: Sau khi đun nhẹ, phản ứng thủy phân diễn ra tạo NaOH làm hoa hồng chỉ thị phenolphthalein.

- Ban đầu:
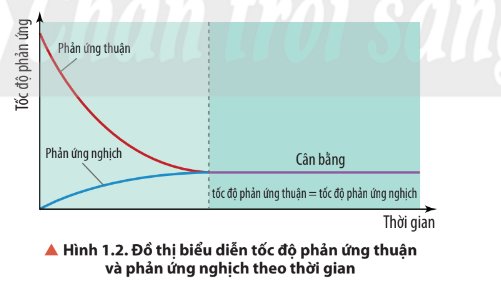
+ Tốc độ phản ứng thuận giảm dần;
+ Tốc độ phản ứng nghịch tăng dần;
- Đến thời điểm cân bằng: Tốc độ phản ứng thuận = tốc độ phản ứng nghịch.

\(\Delta_rH^0_{298}=-1300kJ\) nên phản ứng là toả nhiệt.
Nhiệt lượng toả ra là 1 300 kJ nên dễ dàng thấy được phản ứng trên xảy ra thuận lợi. Hay ethanol dễ cháy, khi cháy toả nhiều nhiệt.

tham khảo.
Hiện tượng: Cây nên đang cháy bị tắt khi đặt trong bình kín chứa khí nitrogen.
Giải thích: Khí nitrogen không có khả năng duy trì sự cháy.

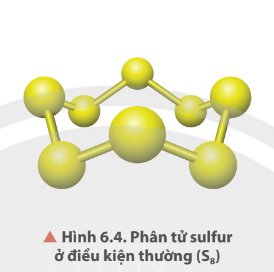
Ở dạng phân tử, sulfur gồm 8 nguyên tử liên kết cộng hoá trị với nhau tạo thành mạch vòng.




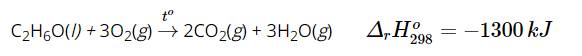


- Chuỗi 1:
(1) \(CH_3COONa+NaOH\underrightarrow{^{t^o,CaO}}CH_4+Na_2CO_3\)
(2) \(C_4H_{10}\underrightarrow{^{t^o,p,xt}}CH_4+C_3H_6\)
(3) \(Al_4C_3+12H_3O\rightarrow4Al\left(OH\right)_3+3CH_4\)
(4) \(2CH_4\underrightarrow{^{1500^oC,lln}}C_2H_2+3H_2\)
(5) \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
(6) \(CH_4+Cl_2\underrightarrow{^{as}}CH_3Cl+HCl\)
(7) \(CH_3Cl+Cl_2\underrightarrow{^{as}}CH_2Cl_2+HCl\)
(8) \(CH_4+O_2\underrightarrow{^{t^o,xt}}HCHO+H_2O\)
- Chuỗi 2:
(1) \(C_2H_2+H_2\underrightarrow{^{t^o,Pd}}C_2H_4\)
(2) \(nCH_2=CH_2\underrightarrow{^{t^o,p,xt}}\left(-CH_2-CH_2-\right)_n\)
(3) \(3C_2H_4+2KMnO_4+4H_2O\rightarrow3C_2H_4\left(OH\right)_2+2MnO_{2\downarrow}+2KOH\)
(4) \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
(5) \(C_2H_4+H_2O\underrightarrow{^{t^o,xt}}C_2H_5OH\)
(6) \(C_2H_5OH\xrightarrow[170^oC]{^{H_2SO_4\left(đ\right)}}C_2H_4+H_2O\)
(7) \(C_2H_4+H_2\underrightarrow{t^o,Ni}C_2H_6\)
(8) \(C_2H_6\underrightarrow{t^o,p,xt}C_2H_4+H_2\)
(9) \(C_2H_4+HCl\underrightarrow{t^o,xt}C_2H_5Cl\)
(10) \(C_2H_6+Cl_2\underrightarrow{as}C_2H_5Cl+HCl\)
- Chuỗi 3:
(1) \(2CH_4\underrightarrow{^{1500^oC,lln}}C_2H_2+3H_2\)
(2) \(CaC_2+2H_2O\rightarrow C_2H_2+Ca\left(OH\right)_2\)
(3) \(C_2H_2+2H_2\underrightarrow{^{t^o,Ni}}C_2H_6\)
(4) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
(5) \(C_2H_2+H_2O\underrightarrow{t^o,xt}CH_3CHO\)
(6) \(C_2H_2+HCl\underrightarrow{t^o,xt}CH_2=CHCl\)
(7) \(nCH_2=CHCl\underrightarrow{t^o,p,xt}\left(-CH_2-CHCl-\right)_n\)
(8) \(2C_2H_2\underrightarrow{t^o,p,xt}C_4H_4\)
(9) \(3C_2H_2\underrightarrow{t^o,p,xt}C_6H_6\)
(10) \(C_2H_2+2AgNO_3+2NH_3\rightarrow Ag_2C_2+2NH_4NO_3\)