Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cứu em với, giải đầy đủ xíu.
Bài bạn làm cho em là bài 4 đó, bài 3 bạn ghi lộn bài 4 á.
Cứu em với, giải đầy đủ xíu.
Bạn dưới giúp em bài 4
Anh giúp em bài 3.
---
Ta có: nP= mP/M(P)=6,2/31=0,2(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: nO2= 5/4 . nP= 5/4 . 0,2= 0,25(mol)
=> V(O2,đktc)=nO2.22,4= 0,25.22,4= 5,6(l)
Giả sử: V(O2,đktc)=1/5. Vkk
=> Vkk=5.V(O2,đktc)=5.5,6=28(l)

Cứu em với, giải đầy đủ xíu. theo PTHH đó e
hệ số của Fe2O3 là 1
hệ số của H2 là 3
->n H2=3n Fe2O3
dùng tỉ lệ của hệ số
VD: Tỉ lệ hệ số của Fe2O3 và H2 là 1/3
=> Tỉ lẹ số mol = 1/3 => nFe2O3 = 1/3nH2
=> nH2 = 0,1 : 1/3 = 0,3 (mol)

a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right);n_{H_2SO_4}=0,1.0,5=0,05\left(mol\right)\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Theo đề:0,2......0,05
Lập tỉ lệ: \(\dfrac{0,2}{2}>\dfrac{0,05}{3}\)=> Al dư, H2SO4 hết
=> \(V_{H_2}=0,05.22,4=1,12\left(l\right)\)
=> Chọn C
b) \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}n_{H_2SO_4}=\dfrac{0,05}{3}=\dfrac{1}{60}\left(mol\right)\)
=> \(C_{M\left(Al_2\left(SO_4\right)_3\right)}=\dfrac{1}{\dfrac{60}{0,1}}==0,17M\)
=> Chọn A

\(\dfrac{2A}{2A+16.5}=\dfrac{43,66}{100}\)
=> \(200A=43,66.\left(2A+16.5\right)\)
=> \(200A-87,32A=3492,8\)
=> \(112,68A=3492,8\)
=> A= 31

bạn bấm máy tính hoặc giải hệ:
\(\left\{{}\begin{matrix}27x+56y=11\\1,5x+y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}27x+56y=11\\84x+56y=22,4\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}57x=11,4\\27x+56y=11\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\27.0,2+56y=11\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)

Câu 3:
a) Lưu huỳnh (S) có hóa trị II. Hidro (H) có hóa trị I.
-> Ta sẽ có hợp chất: \(H^I_aS^{II}_b\) (a,b: nguyên, dương)
Theo quy tắc hóa trị ta có:
I.a=II.b
=>a/b=II/I=2/1
=>a=2; b=1
=> CTHH là H2S
Câu 3b)
- Na có hóa trị (I) và CO3 có hóa trị (II).
- Ta đặt: \(Na^I_x\left(CO_3\right)^{II}_y\) (x,y: nguyên, dương)
Theo QT hóa trị ta sẽ có được:
x.I=II.y
<=>x/y=II/I=2/1
=>x=2; y=1
=> CTHH sẽ là Na2CO3


\(S_{CuSO_4\left(t^o=10^oC\right)}=17,4\left(g\right)\) Đề cho sai rồi
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(n_{H_2SO_4}=n_{CuSO_4}=0,2\left(mol\right)\)
\(m_{H_2SO_4}=0,2.98=19,6\left(g\right)\)
\(m_{dd\left(H_2SO_4\right)}=\dfrac{19,6}{20}.100=98\left(g\right)\)
\(m_{CuSO_4}=0,2.160=32\left(g\right)\)
Khối lượng dung dịch sau khi hòa tan CuO:
\(0,2.80+98=114\left(g\right)\)
Khối lượng nước có trong dung dịch:
\(114-32=82\left(g\right)\)
Gọi a là số mol CuSO4.5H2O tách ra
Khối lượng CuSO4 còn lại trong dung dịch là: 32- 160a
Khối lượng H2O còn lại trong dung dịch là: 82 – 90a
Vì độ tan của CuSO4 ở 100C là 17,4 gam nên ta có:
\(\dfrac{32-160a}{82-90a}=\dfrac{17,4}{100}\)
\(\Rightarrow a\simeq0,12285\left(mol\right)\)
Khối lượng tinh thể đã tách ra: \(0,12285.250=30,7125g\)


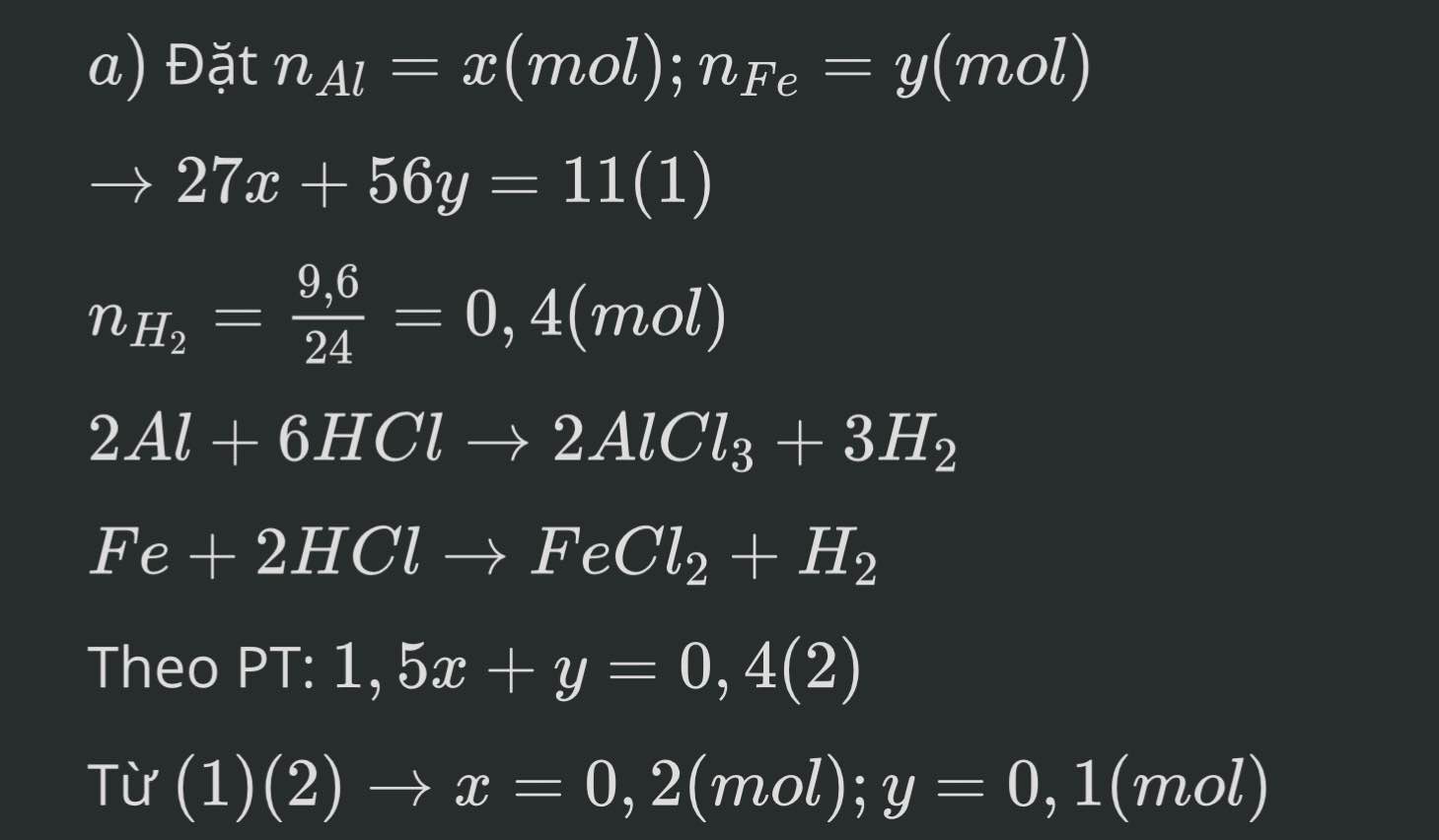



 n giúp em với ạ giải chi tiết ạ
n giúp em với ạ giải chi tiết ạ
Câu 1 em mở SGK nha
Câu 2:
a) Fe2O3 + 3 H2 -to-> 2 Fe + 3 H2O
b) HgO + H2 -to->Hg + H2O
c)PbO + H2 -to-> Pb + H2O
Câu 3:
nHgO= 21,7/217=0,1(mol)
PTHH: HgO + H2 -to-> Hg + H2O
0,1________0,1_______0,1(mol)
a) nHg= 0,1.201=20,1(g)
b)mH2=0,1.2=0,2(g)
V(H2,đktc)=0,1.22,4=2,24(l)
4)
nH2= 8,4/22,4=0,375(mol)
PTHH: H2 + 1/2 O2 -to-> H2O
0,375__________________0,375
=>mH2O=0,375.18= 6,75(g)
Cảm ơn anh ạ <3