Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2Cu+O2=>2CuO
khối lượng tăng lên chính là khối lượng CuO tạo thành
gọi khối lương Cu ban đầu là a gam
=> khối lượng tăng lên (CuO) là 1/6*a
=>khối lượng chất rắn sau phản ứng là 7/6*a
% khối lượng của chất sắn thu được sau khi nung là:
(1/6a)/(7/6a)*100%=\(\frac{\frac{1}{6}}{\frac{7}{6}}\cdot100\%\) xấp xỉ 14pt
( mình nghĩ chắc là đúng ==)

Gọi x là số mol CuO tham gia pư
ylà số mol CuO dư
CuO+H2----->Cu+H2O
x x x
Ta có hệ PT:
(x+y)80=28
64x+80y=24
\(\Rightarrow\) x=0,25;y=0,1
mH2O=0,25*18=4,5g

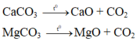
Gọi số mol C a C O 3 và M g C O 3 lần lượt là a và b mol
→ 100a + 84b = 30 (gam) (1)
Theo bài ra khối lượng chất rắn sau phản ứng là 30 : 2 = 15 gam
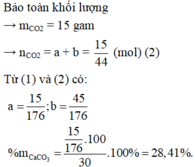
⇒ Chọn A.

Cau 1 :
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,1
a) Chat trong dung dich A thu duoc la : sat (II) clorua
Chat ran B la : dong
Chat khi C la : khi hidro
b) \(n_{Fe}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(m_{Cu}=10-5,6=4,4\left(g\right)\)
0/0Fe = \(\dfrac{5,6.100}{10}=56\)0/0
0/0Cu = \(\dfrac{4,4.100}{10}=44\)0/0
c) Co : \(m_{Cu}=4,4\left(g\right)\)
\(n_{Cu}=\dfrac{4,4}{64}=0,06875\left(mol\right)\)
Pt : \(Cu+2H_2SO_{4dac}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
0,06875 0,06875
\(n_{SO2}=\dfrac{0,06875.1}{1}=0,06875\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=1,54\left(l\right)\)
Chuc ban hoc tot
Minh xin loi ban nhe , ban bo sung vao cho :
\(V_{SO2\left(dktc\right)}=0,06875.22,4=1,54\left(l\right)\)

a)
$2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2$
Gọi $n_{CuO} = n_{Cu(NO_3)_2\ pư} = a(mol)$
Suy ra:
$m_{giảm} = 188a - 80a = 54 \Rightarrow a = 0,5(mol)$
$m_{Cu(NO_3)_2\ pư} = 0,5.188 = 94(gam)$
b)
$n_{NO_2} = 4a = 2(mol)$
$n_{O_2} = 0,5a = 0,25(mol)$
$V_{NO_2} = 2.22,4 = 44,8(lít)$
$V_{O_2} = 0,25.22,4 = 5,6(lít)$


Như vậy khi phản ứng Cu xảy ra hoàn toàn thì khối lượng tăng lên 1/4
Theo đề bài, sau phản ứng khối lượng chất rắng
Cu tăng lên 1/6 khối lượng bạn đầu => Cu chưa bị oxi hóa hết thu được CuO và Cu còn dư
Giả sử thí nghiệm với 128 Cu. Theo đề, g oxi phản ứng:
128/6 = 21,333 g
Theo PTHH của phản ứng số g Cu đã phản ứng với số g oxi và số g CuO được tạo thành:
128.32 . 21,333 = 85,332 g ; mCuO = 160/32 21,333 = 106,665 g
Số g Cu còn lại :
128 - 85,332 = 42,668 g
%Cu = \(\frac{42,668}{149,333}100=28,57\%\) => %CuO = 71,43%
tai sao la 1/4