
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


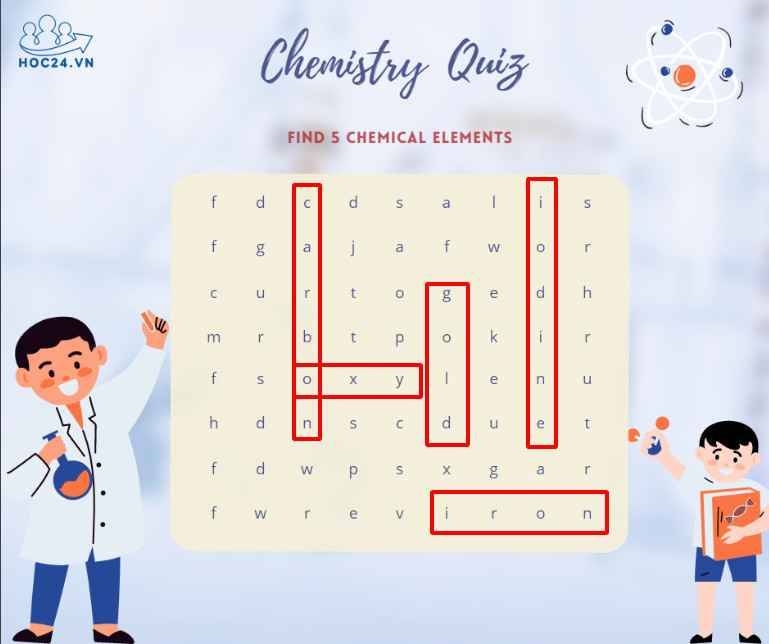
*cái oxy em k chắc á cô:<< em tìm được mấy nguyên tố này th ạ:<.

Đề bài cho hỗn hợp X gồm hai khí là methane (CH4) và ethylene (C2H4). Hỗn hợp này có tỉ khối so với hydrogen (H2) bằng 10.
- Bước 1: Tính khối lượng mol trung bình của hỗn hợp X (MX)
Tỉ khối của hỗn hợp X so với hydrogen được tính bằng công thức: dX/H2=MH2MX.
Trong đó, MH2=2 g/mol.
Ta có: 10=2MX⇒MX=10×2=20 g/mol.
- Bước 2: Gọi thành phần phần trăm thể tích của từng khí trong hỗn hợp
Giả sử trong 1 mol hỗn hợp X, số mol của CH4 là x và số mol của C2H4 là y.
Ta có: x+y=1 (1)
Khối lượng mol trung bình của hỗn hợp X được tính bằng công thức: MX=nCH4+nC2H4nCH4⋅MCH4+nC2H4⋅MC2H4.
MCH4=12+4=16 g/mol.
MC2H4=12×2+4=28 g/mol.
Thay vào công thức ta có: 20=x+yx⋅16+y⋅28=116x+28y (2)
Từ (1) và (2) ta có hệ phương trình:
x+y=1
16x+28y=20
Giải hệ phương trình này, ta được: x=32 và y=31.
Điều này có nghĩa là trong hỗn hợp X, số mol của CH4 chiếm 32 và số mol của C2H4 chiếm 31.
- Bước 3: Tính tổng số mol của hỗn hợp X
Thể tích của hỗn hợp X ở điều kiện tiêu chuẩn (đktc) là 3,7185 lít.
Số mol của hỗn hợp X là: nX=24.79V=24.793.7185=0.15 mol.
(Lưu ý: Nếu đề bài cho ở điều kiện tiêu chuẩn cũ (0 độ C, 1 atm) thì V = 22.4, nhưng theo quy ước quốc tế mới, 1 bar và 25 độ C thì V = 24.79. Đề bài không nói rõ nên ta chọn chuẩn mới là 24.79).
- Bước 4: Tính số mol C2H4 trong hỗn hợp X
Từ kết quả ở bước 2, ta biết số mol C2H4 chiếm 31 tổng số mol.
nC2H4=nX×y=0.15×31=0.05 mol.
- Bước 5: Tính số mol Br2 đã phản ứng
Khi hỗn hợp X cho qua dung dịch Br2 dư, chỉ có ethylene (C2H4) phản ứng vì nó có liên kết đôi (C=C). Methane (CH4) là ankan nên không phản ứng với Br2.
Phương trình phản ứng:
C2H4+Br2→C2H4Br2
Theo phương trình, tỉ lệ mol là 1:1, vậy:
nBr2=nC2H4=0.05 mol.
Kết luận
Số mol Br2 đã tham gia phản ứng là 0,05 mol.


12.
Na2CO3+H2SO4->Na2SO4+H2O+CO2
............. 0,5 ............. ......... 0,5
CO2+2KOH->K2CO3+H2O
x 2x x
CO2+KOH->KHCO3
y y y
mKOH=98.40/100=39,2g
nKOH=39,2/56=0,7mol
Có:
2x+y=0,7
138x+100y=57,6
=>x=0,2mol; y=0,3mol
mK2CO3=138.0,2=27,6g
mKHCO3=57,6-27,6=30g
b.
nCO2=x+y=0,2+0,3=0,5mol
CMddH2SO4=0,5/0,2=2,5M
8. Hoàn thành sơ đồ chuyển hóa sau:
Mg \(\underrightarrow{\left(1\right)}\) MgO \(\underrightarrow{\left(2\right)}\) MgCl2 \(\underrightarrow{\left(3\right)}\) Mg(OH)2 \(\underrightarrow{\left(4\right)}\) MgO \(\underrightarrow{\left(5\right)}\) MgSO4 \(\underrightarrow{\left(6\right)}\) MgCO3 \(\underrightarrow{\left(7\right)}\) MgO
\(\left(1\right)2Mg+O_2\underrightarrow{t^o}2MgO\)
\(\left(2\right)MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(\left(3\right)MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
\(\left(4\right)Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
\(\left(5\right)MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(\left(6\right)MgSO_4+Na_2CO_3\rightarrow MgCO_3+Na_2SO_4\)
\(\left(7\right)MgCO_3\underrightarrow{t^o}MgO+CO_2\uparrow\)

Câu 3:
N2+O2\(\overset{t^0}{\rightarrow}\)2NO
4NO+3O2+2H2O\(\rightarrow\)4HNO3
NO3- : làm tăng lượng phân đạm cho cây!

PTHH : Al + HCl => AlCl3 + H2
Fe + HCl => FeCl2 + H2
a. nHCl = CM. V = 1.0,7 = 0,7 (mol)
Đặt số mol của Al =x ; Fe =y
PTHH : 2Al +6HCl => 2AlCl3 + 3H2
x -> 3x
Fe + 2HCl => FeCl2 + H2
y -> 2y
Ta có : x.27 + y.56 = 43,9 (g)
3x +2y = 0,7 (mol)
( cậu dùng máy tính giải hệ pt 2 ẩn nhé, tớ hiện không có máy tính )
=> x=...
y=....
Từ x,y suy ra số mol trên 2 pt của H2 rồi cộng lại với nhau => V=n.22,4
b. tính mFe, mAl
%mFe= \(\dfrac{mFe}{43,9}\).100% =
%mAl = \(\dfrac{mAl}{43,9}\).100% =
c.Vdd pư = Vdd bđ =0,7 (l)
CM AlCl3 =\(\dfrac{nAlCl_3}{Vddpư}\)=
CM FeCl2 = \(\dfrac{nFeCl_2}{Vddpu}\)=
Lần sau em nhớ xoay ảnh về đúng chiều để cô và các bạn dễ quan sát câu hỏi nhé

12. Na2O + H2O ---> 2 NaOH
0,4 mol 0,8
CaCO3 ---> CaO + CO2
0,5 mol 0,5
CO2 + 2NaOH ---> Na2CO3 + H2O
0,4 0,8 mol 0,4
CO2 + Na2CO3 + H2O ---> 2NaHCO3
0,1 mol 0,1 0,2
=> Muối thu được có Na2CO3 0,4 - 0,1 = 0,3 mol và NaHCO3 0,2 mol
=> m Muối = 0,3. 106 + 0,2. 84 = 48,6g
11a. CO2 0,1 mol. NaOH 0,1 mol => Sản phẩm sau pư là NaHCO3 0,1 mol
=> m = 0,1.84 = 8,4g.
11b. SO2 0,5 mol. KOH 1,5 mol => Sau pư có K2SO3 0,5 mol và KOH dư 0,5 mol
=> mK2SO3 = 0,5. 158 = 79g và mKOH = 0,5. 56 = 28g.
11c. CO2 = 0,3 mol và Ca(OH)2 0,2 mol
=> sau pư có CaCO3 0,1 mol và Ca(HCO3)2 0,1 mol

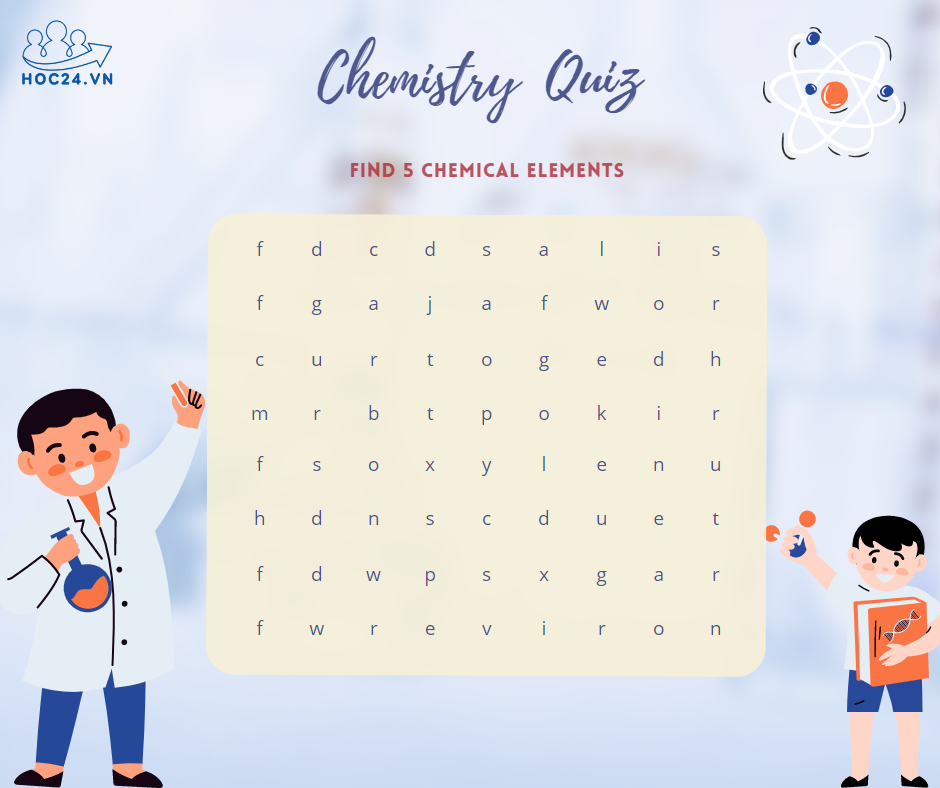
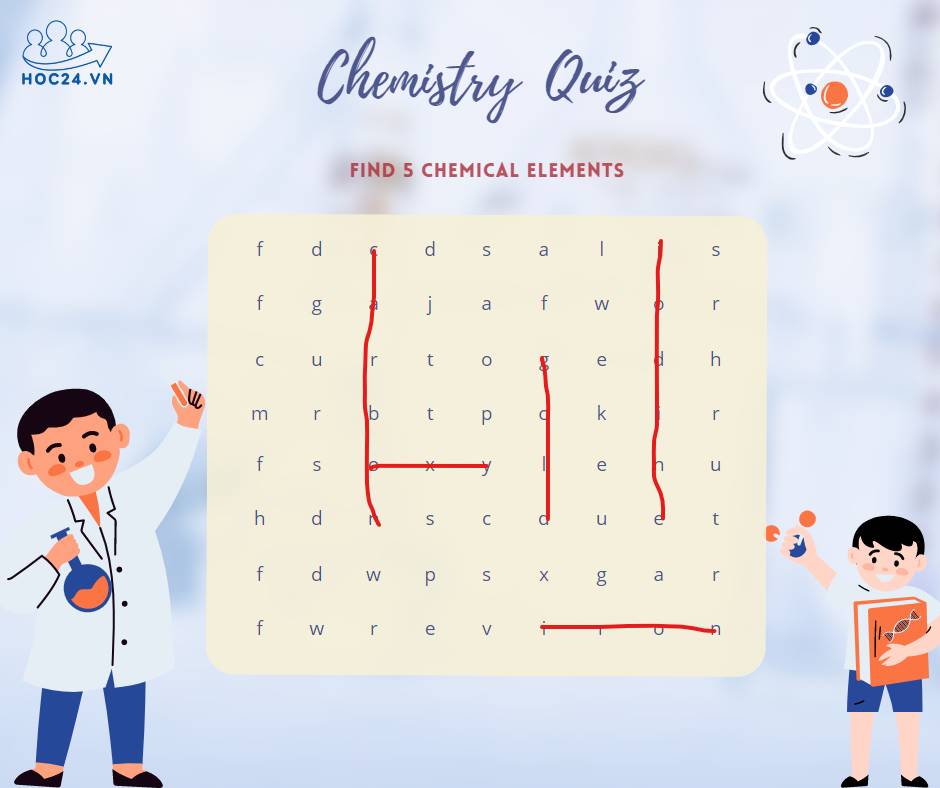















 Giúp mình giải vài câu thực tế Hoá nha..
Giúp mình giải vài câu thực tế Hoá nha..






