
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


câu A:
gọi hóa trị của Fe là x
\(\rightarrow Fe_2^xO_3^{II}\rightarrow x.2=II.3\rightarrow x=\dfrac{VI}{2}=III\)
vậy Fe hóa trị III
câu B:
gọi hóa trị của Zn là x
\(\rightarrow Zn_1^xCl^I_2\rightarrow x.1=I.2\rightarrow x=II\)
vậy Zn hóa trị II

\(a,2Fe(OH)_3\xrightarrow{t^o}Fe_2O_3+3H_2O\\ b,m_{Fe(OH)_3}=m_{Fe_2O_3}+m_{H_2O}\\ c,m_{Fe(OH)_3(p/ứ)}=160+54=214(g)\\ \Rightarrow \%_{Fe(OH)_3(phân hủy)}=\dfrac{214}{400}.100\%=53,5\%\)

Ta có: hóa trị của CO3 bằng hóa trị của O
⇒ Hóa trị của CO3 là II
⇒ Fe có hóa trị II


\(MgS,Mg\left(NO_3\right)_2,MgCO_3,Mg_3\left(PO_4\right)_2\)
\(Fe_2S_3,Fe\left(NO_3\right)_3,Fe_2\left(CO_3\right)_3,FePO_4\)
\(\left(NH_4\right)_2S,NH_4NO_3,\left(NH_4\right)_2CO_3,\left(NH_4\right)_3PO_4\)

b) Ta có : \(M_C=12\) (đvC)
Mà \(M_X=2M_C\)
=> \(M_X=24\)
Vậy X là Magie (Mg), hóa trị II
b)\(M_X=24;M_{Zn}=65\)
\(\Rightarrow M_X=\dfrac{24}{65}M_{Zn}\)
c) Nếu tăng thêm 3đvC thì \(M_X=24+3=27\left(Al\right)\)
=> Z=P=E = 13e
Sơ đồ nguyên tử Al :
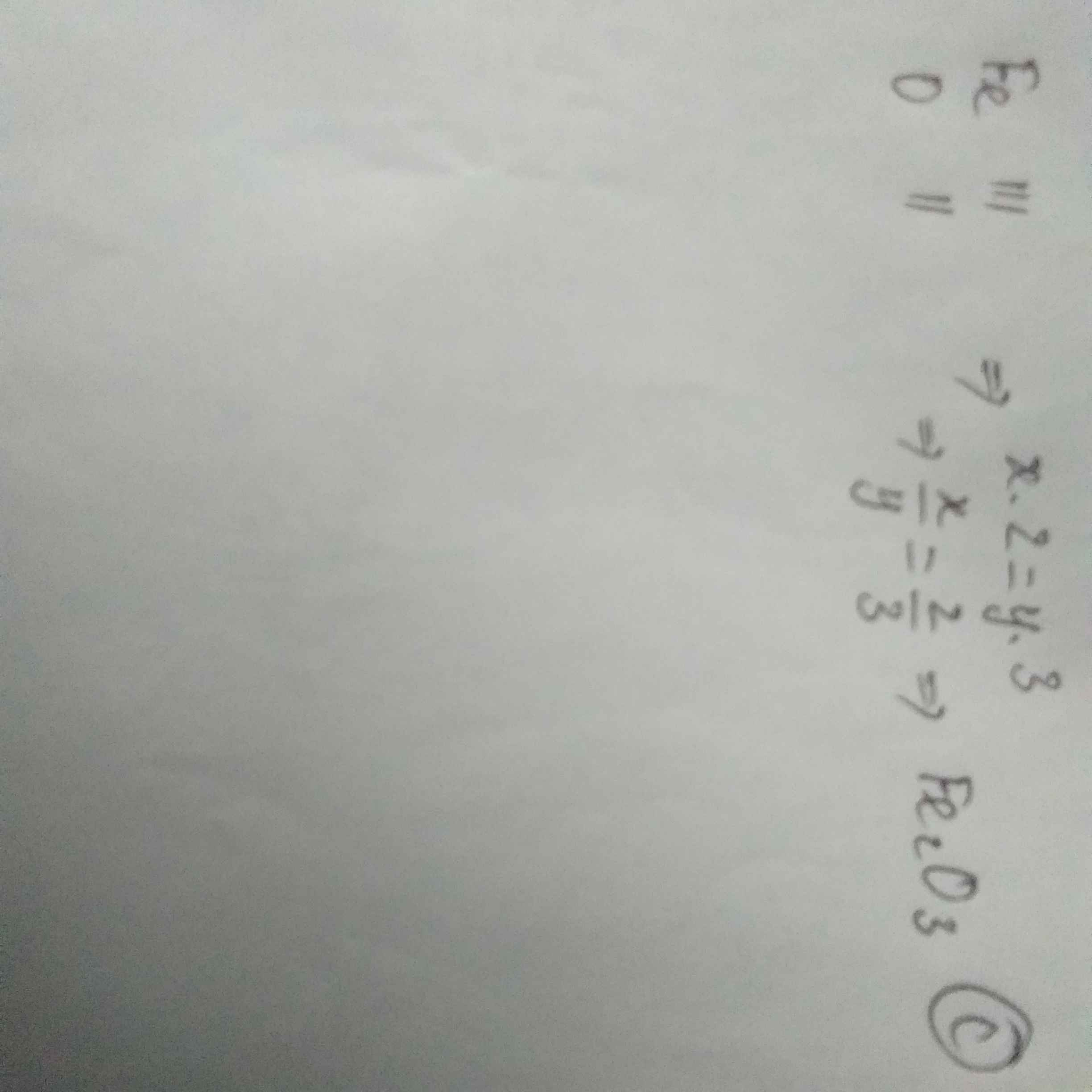
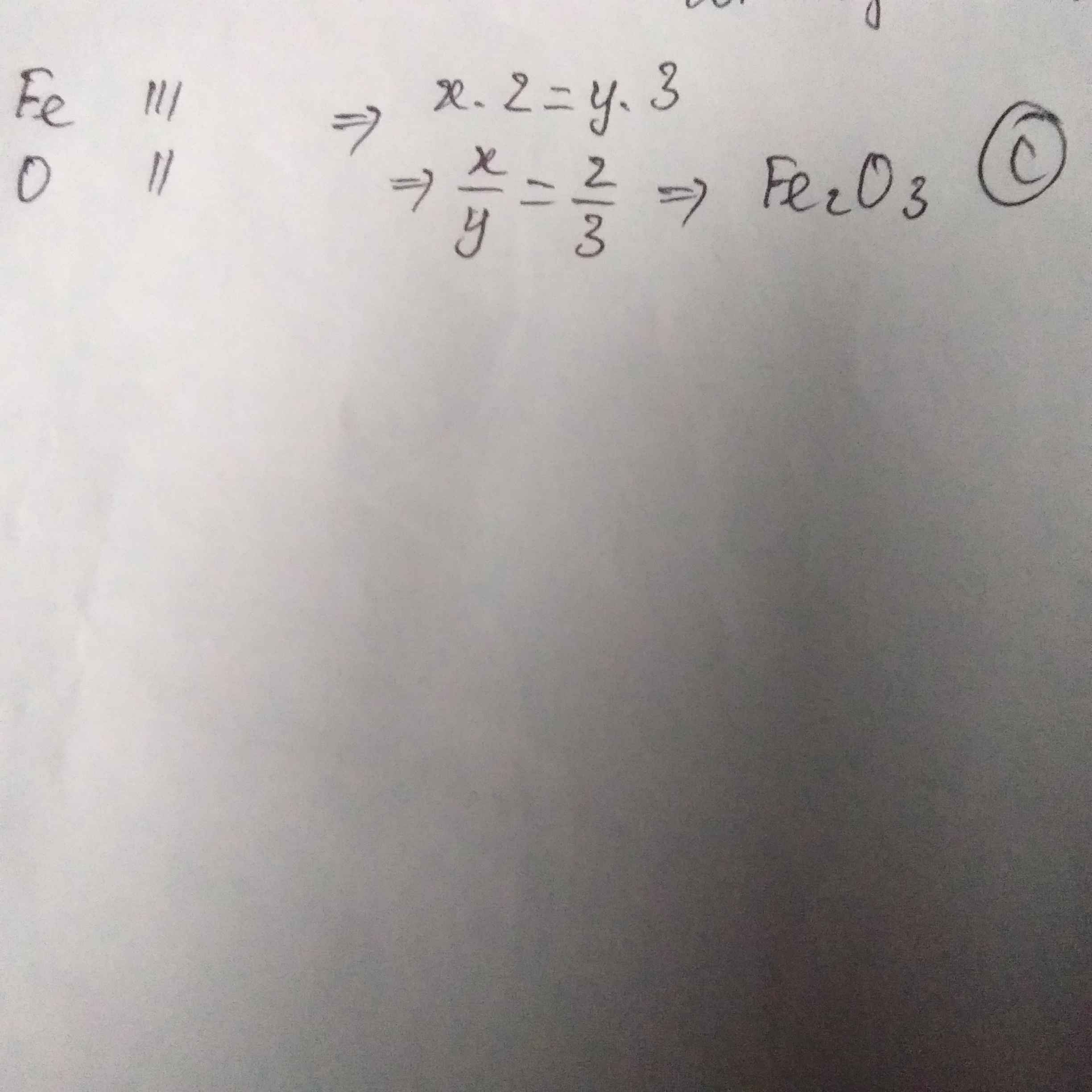
Gọi hóa trị của Fe là x (O có hóa trị II)
Theo quy tắc hóa học
⇒ x.II=2.II
⇒ x=II
⇒Fe có hóa trị II