Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Sự oxi hóa
Fe → Fe2+ + 2e
(vì lượng Fe phản ứng tối đa nên Fe chuyển lên Fe2+).
Sự khử
4H+ + NO3- + 3e → NO + 2H2O
0,08 ← 0,02 → 0,06 → 0,01
Cu2+ + 2e → Cu
0,01 → 0,02
2H+(dư) + 2e → H2
0,02 → 0,02 → 0,01
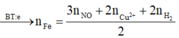
= 0,5 mol => m F e = 2 , 8 ( g )

Đáp án C
3Fe + 8 H + + 2 N O - 3 → 3 F e 2 + + 2NO + 4 H 2 O
0,03 0,08 ← 0,02 mol

=> Lượng Fe hòa tan tối đa
![]()

Đáp án C


Theo đó, bảo toàn nguyên tố Fe có 0,1 mol Fe đơn chất trong X → % m Fe trong X ≈ 37 , 73 %

Đáp án C
![]()
![]()
Ta có sơ đồ phản ứng:
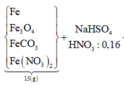
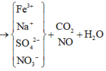
![]()
Bảo toàn e: ![]()
Xét ![]()
![]()
Bảo toàn gốc ![]()
![]()
Bảo toàn điện tích: ![]()
Bảo toàn nguyên tố Hidro: ![]()
Bảo toàn khối lượng: m Z = 4 , 92 ( g ) => dễ giả ra được 0,03 mol C O 2 ; 0,12 mol NO
Bảo toàn nguyên tố Nito:
![]() = 0,03 mol
= 0,03 mol
![]()
![]()
Bảo toàn nguyên tố Fe: ![]()
![]()

Đáp án C
Phân tích: dung dịch Y + Cu → sản phẩm có NO nên Y chứa H+ và NO 3 - → muối sắt chỉ có Fe3+.
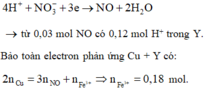
Xử lí Ba(OH)2 + Y: 154,4 gam kết tủa gồm 0,18 mol Fe(OH)3 và ? mol BaSO4 → ? = 0,58 mol.
« Sơ đồ phản ứng chính:

Bảo toàn electron hoặc bảo toàn nguyên tố O (nhớ ghép bỏ cụm) → có 0,01 mol Fe3O4.
Theo đó, bảo toàn nguyên tố Fe có 0,1 mol Fe đơn chất trong X
![]()
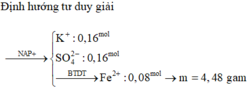

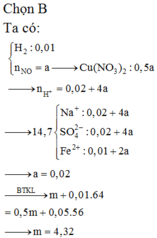
Đáp án C
Sự oxi hóa
Sự khử
Fe → Fe2+ + 2e
(vì lượng Fe phản ứng tối đa nên Fe chuyển lên Fe2+).
4H+ + NO3- + 3e → NO + 2H2O
0,08 ← 0,02 → 0,06 → 0,01
Cu2+ + 2e → Cu 0,01 → 0,02
2H+(dư) + 2e → H2
0,02 → 0,02 → 0,01