Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

H2 + CuO →Cu + H2O (1)
CO + CuO→ Cu + CO2(2)
CO2 + Ca(OH)2→ CaCO3 + H2O
nCaCO3 = nCO2 = 2:100=0,02 mol =nCu(1)=nCO
⇒mCO = 0,02 . 28=0,56g
\(\Sigma\)nCu = 1,92: 64=0,03 mol ⇒nCu(2) = 0,03-0,02=0,01mol=nH2
⇒mH2 = 0,01 . 2 = 0,02g ⇒%mH2=3,4% %mCO=96,6%
VCO2= 0,02 . 22,4=0,448 l

Chọn đáp án B
Ta có: 1 mol dung dịch X chứa x+2y mol OH-
+ Ta có 1 mol dung dịch Y chứa y+2x mol OH-
+ Vì khi cho SO42- vào vẫn còn kết tủa nên lượng kết tủa tính trong bài hoàn toàn tính theo CO32-
+ Hấp thụ hết 0,04 mol CO2 vào 200 ml dung dịch X, thu được dung dịch M và 1,97 gam kết tủa
⇒ nOH– = 0,2×(x+2y)
⇒ nBaCO3 = 0,01, nBa(HCO3)2 = 0 , 04 - 0 , 01 2 = 0,015 mol
⇒ nOH– = 0,01×2 + 0,015×2 = 0,05 mol.
⇒ x + 2y = 0,25.
+ Nếu hấp thụ hết 0,0325 mol CO2 vào 200 ml dung dịch Y thì thu được dung dịch B và 1,4775 gam kết tủa.
nBaCO3 = 0,0075 ⇒ nHCO3– = 0,0325 – 0,0075 = 0,025.
⇒ nOH– = 0,2×(2x + y) = 0,025 + 0,0075×2 = 0,04 → 2x + y = 0,2.
⇒ x = 0,05 và y = 0,1

Số mol CaCO3 là nCaCO3 = 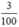 =0,03(mol)
=0,03(mol)
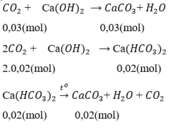
Số mol kết tủa thêm nCaCO3 = 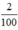 = 0,02 (mol)
= 0,02 (mol)
Theo pt ⇒ nCa(HCO3)2 = nCaCO3 = 0,02 mol
Tổng số mol CO2 = nCO2 (1) + nCO2 (2) = 0,03 + 2. 0,02 = 0,07 (mol)

Chọn đáp án B.
Áp dụng định luật bảo toàn khối lượng có: m Y = m X
⇒ m Y = 44.0 , 08 + 52.0 , 06 + 2.0 , 15 = 6 , 94 g ⇒ n Y = 6 , 94 347 14 .2 = 0 , 14 m o l
n H 2 phan ung = n X − n Y = 0 , 06 + 0 , 06 + 0 , 15 − 0 , 14 = 0 , 15 m o l
Þ H2 phản ứng hết.
Kết tủa A gồm Ag, A g C ≡ C C H = C H 2 , AgC ≡ CCH 2 CH 3
Có 5 6 .0 , 12 = 0 , 1 > 0 , 06 ⇒ Chứng tỏ có 0,1 mol Ag (tạo bởi 0,05 mol CH3CHO dư).
Đặt số mol của A g C ≡ C C H = C H 2 , AgC ≡ CCH 2 CH 3 lần lượt là a, b
⇒ a + b = 0 , 12 − 0 , 1 = 0 , 02 m o l (1)
Áp dụng định luật bảo toàn liên kết π có: 0 , 08 + 3.0 , 06 = 0 , 15 + 0 , 06 + 3 a + 2 b
⇒ 3 a + 2 b = 0 , 05 (2)
Từ (1) và (2) suy ra a = b = 0 , 01
⇒ m ket tua = 108.0 , 1 + 159.0 , 01 + 161.0 , 01 = 14 g
Gần nhất với giá trị 14,1

Đáp án B
Coi phản ứng của 0,04 mol CO2 với dung dịch X là thí nghiệm 1 (TN1); phản ứng của Y với 0,0325 mol CO2 là thí nghiệm 2 (TN2).
Ở cả hai TN n BaCO 3 < n CO 2 . Mặt khác, dung dịch sau phản ứng ở hai TN phản ứng với KHSO4 đều tạo ra kết tủa. Suy ra : Dung dịch sau phản ứng còn chứa Ba2+. Ion CO 3 2 - tạo ra đã chuyển hết vào BaCO3. Dung dịch sau các phản ứng chứa
![]()
Sử dụng bảo toàn nguyên tố Ba, C và bảo toàn điện tích cho dung dịch sau phản ứng, ta có:
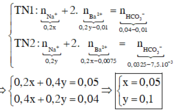

Đáp án : A
Ta có : n CaCO3 = 2/100 = 0,02 mol ≠ n CaCO3 =0,03 mol
Xét 2 Trường hợp :
TH1 : chỉ xảy ra phản ứng tạo CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,02 0,02
=> n CO2 = n CaCO3 =0,02 mol
TH2 : xảy ra 2 phản ứng tạo muối CaCO3và Ca(HCO3)2
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
0,02 0,02
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,02 0,01
Theo phản ứng (1)và (2) : n CO2 p/ứ= 0,02 + 0,02 = 0,04 mol
=> Đáp án A
CÁCH khác : sử dụng phương pháp đồ thị :
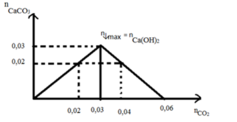
Dựa vào đồ thị => n CO2 = 0,02 mol hoặc 0,04 mol

Đáp án B
![]()
![]()
Bảo toàn khối lượng:
![]()
![]()
Bảo toàn nguyên tố Hidro: ![]()
Bảo toàn nguyên tố Nito: ![]()
![]()
![]()
Đặt ![]()
![]()
Bảo toàn e: ![]()
![]()
Bảo toàn nguyên tố Clo:
![]()
![]()
= 289,31 (g)
Giải hệ: ![]()
![]()
search trc khi hỏi : X chứa a mol Ca(OH)2.cho X hấp thụ qua CO2 0.06 mol thu được 2b mol kết tủa? | Yahoo Hỏi & Đáp