
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án là B.
Sau phản ứng thu được hỗn hợp kim loại nên Fe dư.
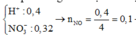
V = 22,4 (l)
![]()
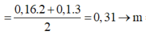
= 17,8 - 0,31.56 + 0,16.64 = 10,68 (g)

Đáp án C
Phương pháp: Viết PTHH. Chú ý do sau phản ứng thu được hỗn hợp kim loại nên Fe dư, phản ứng không tạo Fe3+, chỉ tạo Fe2+.
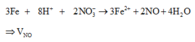
mchất rắn = m Fe dư + mCu => m - 0,07.56 + 64.0,04 = 0,75m => m
Hướng dẫn giải:
H+: 0,08
NO3-: 0,08
Cu2+: 0,04
3Fe + 8H+ + 2NO3-→3Fe2+ + 2NO+4H2O
0,03 0,08 0,02
Fe + Cu2+→ Fe2++Cu
0,04 0,04 0,04
m chất rắn = m Fe dư + mCu => m - 0,07.56 + 64.0,04 = 0,75m
=> m = 5,44 gam
VNO = 0,02.22,4 = 0,448 lít

Đáp án D
Trong phản ứng của Fe với dung dịch X, chất khử là Fe, chất oxi hóa là NO 3 - / H + , Fe3+ và Cu2+. Sau phản ứng thu được hỗn hợp kim loại, chứng tỏ Fe dư nên muối tạo thành trong dung dịch là Fe2+.
Áp dụng bảo toàn electron trong phản ứng của Fe với dung dịch X, bảo toàn điện tích trong dung dịch Y và bảo toàn nguyên tố Fe, N, ta có :
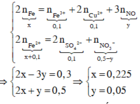
Theo bảo toàn khối lượng, ta có :


Đáp án A
I = 2,68 A; t = 6h ; nKhí = 4,48/22,4 = 0,2 (mol)
![]()
Tại catot xảy ra quá trình oxi hóa Cu2+ Tại anot xảy ra quá trình oxi hóa Cl-, H2O
Cu2+ +2e → Cu 2Cl- → Cl2 + 2e
a → 0,5a → 2a (mol)
2H2O → O2 + 4H+ + 4e
b → 0,5b → 2b → 2b (mol)
Vì dung dịch sau phản ứng tác dụng được với Fe và rắn thu được gồm 2 kim loại => Cu2+ còn dư sau quá trình điện phân. Và có khí NO thoát ra => tại anot H2O bị điện phân để sinh ra H+
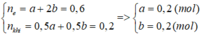
=> nH+ = 2b = 0,4 (mol)
Vì Fe dư sau phản ứng nên Fe chỉ lên số oxi hóa +2; gọi số mol Cu2+ dư là x (mol)
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,15 ← 0,4 (mol)
Fe + Cu2+ → Fe2+ + Cu↓
x ← x → x (mol)
Khối lượng kim loại giảm: ∆ giảm = mFe phản ứng – mCu sinh ra
=> (20 – 12,4) = 0,15 + x).56 – 64x
=> x = 0,1 (mol)
=> nCu2+ bđ = nCu2+ đp + nCu2+ dư = 0,6/2 + 0,1 = 0,4 (mol)
=> m = mCu(NO3)2 + mNaCl = 0,4. 188 + 0,2. 58,5 = 86,9 (g)