Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Từ dữ kiện số mol Ba(OH)2 và BaCO3 chưa đủ để kết luận Co2 dư đâu nha em
\n
$CO + O_{oxit} \to CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{O(oxit)} = n_{CaCO_3} = \dfrac{8}{100} = 0,08(mol)$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$n_{Fe} = n_{H_2} = \dfrac{1,344}{22,4} = 0,06(mol)$
Ta có :
$n_{Fe} : n_O = 0,06 : 0,08 = 3 : 4$
Vậy oxit là $Fe_3O_4$
Công thức oxit sắt có dạng: \(Fe_xO_y\)
\(Fe_xO_y+yCO\rightarrow xFe+yCO_2\uparrow\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(\Rightarrow n_{Fe}=n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
\(\Rightarrow n_{CO}=n_{CO_2}=n_{CaCO_3}=0,08\left(mol\right)\)
\(\Rightarrow n_{O\left(Fe_xO_y\right)}=n_{O\left(CO_2\right)}-n_{O\left(CO\right)}=2n_{CO_2}-n_{CO}=0,08\left(mol\right)\)
\(\Rightarrow n_{Fe}:n_O=0,06:0,08=3:4\)
\(\Rightarrow Fe_3O_4\)

Câu 1
a)
Khí sinh ra là CO2 :
CO+ O→CO2
nBa(OH)2= 0,1 mol
\(n_{BaCO3}=\frac{9,85}{197}=0,05\left(mol\right)\)
Ta có 2 trường hợp:
TH1: Tạo 1 muối trung hòa
Ba(OH)2+ CO2→ BaCO3↓+H2O
_________0,05____0,05
⇒nCO2= 0,05 ⇒nO(FexOy)= 0,05 (1)
TH2: Tạo 2 muối
Ba(OH)2+ CO2→ BaCO3↓+H2O
0,1_____0,1______0,1
CO2+ BaCO3+H2O→ Ba(HCO3)2
0,05___0,05
⇒nCO2= 0,1+0,05= 0,15 mol ⇒nO(FexOy)= 0,15 (2)
PTHH:
Fe+ 2HCl→ FeCl2+H2↑
\(n_{FeCl2}=\frac{12,7}{127}=0,1\left(mol\right)\)
⇒ nFe= 0,1 mol
Vậy với nO= 0.05; nFe= 0,1⇒ x : y= 2:1 (loại)
với nO=0,15; nFe= 0,1⇒ x: y= 2:3 hay CTHC: Fe2O3
b)
m= 0,1.56+0,15.16=8 g
\(V=\frac{0,1.120}{2.100}=0,06l=60l\)
Câu 2:
nCO2= nBaCO3= \(\frac{27,58}{197}\)= 0,14 mol
CO+ O= CO2
\(\rightarrow\) nO (oxit)= nCO2= 0,14 mol
\(\rightarrow\)mO= 0,14.16= 2,24g
Coi oxit kim loại M gồm M và O
\(\rightarrow\) mM= 8,12-2,24= 5,88g
2M+ 2xHCl\(\rightarrow\) 2MClx+ xH2
nH2=\(\frac{2,352}{22,4}\)= 0,105 mol
\(\rightarrow\) nM= \(\frac{0,21}{x}\) mol
\(\rightarrow\)MM= \(\frac{5,88x}{0,21}\)= 28x
x=2 \(\rightarrow\) M=56. Vậy M là sắt (Fe)
FexOy+ yCO\(\underrightarrow{^{to}}\) xFe+ yCO2
nCO2= 0,14 mol \(\rightarrow\)nFexOy= 0,14/y mol
\(\rightarrow\)M FexOy= \(\frac{8,12y}{0,14}\)= 58y
Ta có pt: 56x+16y=58y
\(\Leftrightarrow\) 56x-42y=0
x=3\(\rightarrow\) y=4. Vậy CTHH oxit sắt laf Fe3O4

n(H2)=1,68/22=0,075m0l
n(CaC03)=10/1O0=0,1m0l
gọi công thức oxit sát là FexOy
Ptpu:
Fex0y + yCO ===> xFe + yC02 (1)
Fe + 2HCL ===> FeCl2 + H2
0,075m0l <-----. . . . . . . . . . ---- 0,075m0l
C02 + Ca(0H)2 ===> CaC03 + H20
0,1m0l <-----. . . . . . . . . . 0,1m0l
Theo tỉ lệ số mol theo phương trình (1) ta co:
x/y=n(Fe)/n(C02)=0,075/0,1=3/4
Vay oxit sat can tim la oxit sat tu Fe304
Than yC02
0,15/x(m0l) <=== 0,15
Theobài thì khối lượng oxit sắt oh 2 p/u = nhau nên số mol = nhau hay (0,225/y)=(0,15/x)
<=>0,225x=0,15y
<=>x=2y/3
<=>x/y=2/3
Vậy oxit có công thức là Fe203



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

a) \(CuO+CO\underrightarrow{t^o}Cu+CO2\)
\(FexOy+yCO\underrightarrow{t^o}xFe+yCO2\)
\(Fe+2HCl\rightarrow FeCl2+H2\)
Ta có:
\(n_{H2}=\dfrac{4,704}{22,4}=0,21\left(mol\right)\)
\(\Rightarrow n_{Fe}=0,21\left(mol\right)\Rightarrow m_{Fe}=11,76\left(g\right)\)
\(\Rightarrow m_{Cu}=14,32-11,76=2,56\left(g\right)\)
\(\Rightarrow n_{Cu}=\dfrac{2,56}{64}=0,04\left(mol\right)\)
\(\Rightarrow n_{CuO}=0,04\left(mol\right)\)
\(\Rightarrow\%m_{CuO}=\dfrac{0,04.80}{19,44}.100\%=16,46\%\)
\(\Rightarrow\%m_{FexOy}=100-16,46=83,54\%\)
b) \(m_{FexOy}=19,44-0,04.80=16,24\left(g\right)\)
\(n_{Fe}=0,21\left(mol\right)\)
\(\Rightarrow n_{FexOy}=\dfrac{1}{x}n_{Fe}=\dfrac{0,21}{x}\left(mol\right)\)
\(M_{FexOy}=\dfrac{16,24}{\dfrac{0,21}{x}}=\dfrac{232}{3}x\)
| x | 1 | 2 | 3 |
| \(M_{FexOy}\) | 77,33(loại) | 154,6(loại) | 232(TM) |
\(\Rightarrow FexOy\) là \(Fe3O4\)
Chúc bạn học tốt ^^
Câu a tính khối lượng mỗi chất trong hh ban đầu phải không ạ?
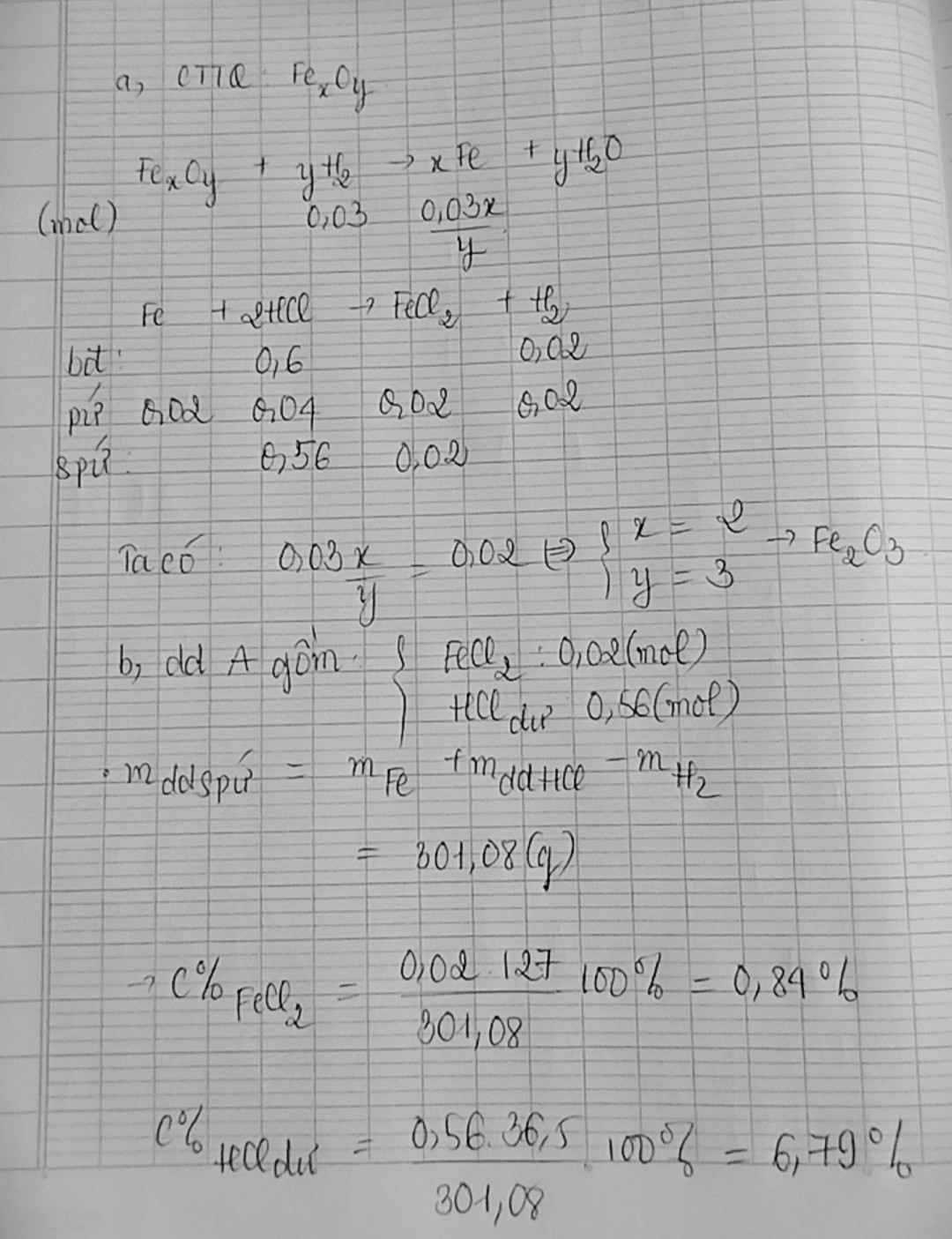
Gọi công thức oxit là FexOy
Ta có : FexOy + xCO \(\underrightarrow{t0}\) xFe + yCO2
Theo đề ta có : \(\left\{{}\begin{matrix}nBa\left(OH\right)=0,1.1=0,1\left(mol\right)\\nBaCO3=\dfrac{9,85}{197}=0,05\left(mol\right)\end{matrix}\right.\)
Ta có PTHH :
Ba(OH)2 + CO2 \(\rightarrow\) BaCO3 \(\downarrow\) + H2O
0,1mol...........0,1mol.....0,1mol
Vì Số mol của BaCO3 còn nên ta có PT :
BaCO3 + H2O + CO2 \(\rightarrow\) Ba(HCO3)2
0,05mol...............0,05mol....0,05mol
=> nCO2 = 0,1+ 0,05 = 0,15 (mol)
Ta có : nCO2 = nO(trong oxit sắt) = 0,15 (mol)
Mặt khác hòa tan tòan bộ m gam bột sắt oxit trên bằng dd HCl dư
FexOy + 2y HCl \(\rightarrow\) x FeCl2y/x + y H2O
thì có sự trao đổi giữa O(trong oxit) vs Cl( trong muối) hay O(-2) với Cl(-)
=> nCl = 2
=> nCl = 2.nO = 2.0,15 = 0,3 (mol)
Theo bảo toàn nguyên tố Cl ta có :
mFe = mFeCl - mCl = 16,25 - 10,65 = 5,6 (g)
=> nFe = \(\dfrac{5,6}{56}=0,1\left(mol\right)\)
Ta có : \(\dfrac{nFe}{nO}=\dfrac{x}{y}=\dfrac{0,1}{0,15}=\dfrac{2}{3}\) => x = 2 ; y= 3
=> CTHH của oxit sắt là Fe2O3
Ta có : nFe2O3 = 1/3nCO2 = 1/3.0,15 = 0,05 (mol)
=> mFe2O3 = 0,05.160 = 8 (g)
Vậy...............