Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Trên nhãn một chai cồn y tế có ghi: Cồn 70o
- Ý nghĩa: Trong 100 ml cồn 70o có 70 ml rượu etylic và 30 ml nước.
Thể tích rượu etylic nguyên chất có trong 50 ml cồn 70o là
- \(V_{C_2H_5OH}=\frac{Đr}{100^0}\times V_{dd C_2H_5OH}=\frac{70^0}{100^0}\times50=35\left(ml\right)\)
b) nC2H5OH = 0,2 mol; nCH3COOH = 0,1 mol
PTHH: CH3COOH + C2H5OH CH3COOC2H5 + H2O
Theo PTHH 1 mol 1 mol
Theo đề bài 0,1 mol 0,2 mol
Ta thấy \(\frac{0,1}{1}< \frac{0,2}{1}\)
Vậy CH3COOH phản ứng hết nếu H =100%. C2H5OH dư, mọi tính toán theo số mol của CH3COOH.
Theo PTHH: \(n_{CH_3COOC_2H_5}=n_{CH_3COOH}=0,1\left(mol\right)\)
\(\Rightarrow m_{CH_3COOC_2H_5\left(LT\right)}=0,1\times88=8,8\left(gam\right)\)
Hiệu suất của phản ứng là: \(Hs=\frac{5,28}{8,8}\times100=60\%\)

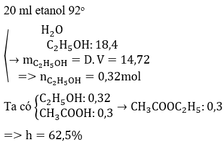
nC2H5OH = 8.05/46 = 0.175 (mol)
nCH3COOH = 36/60 = 0.6 (mol)
nCH3COOC2H5 = 12.32/88 = 0.14 (mol)
C2H5OH + CH3COOH <-H2SO4đ,t0-> CH3COOC2H5 + H2O
1.......................1
0.175................0.6
LTL : 0.175/1 < 0.6/1
=> CH3COOH dư
mCH3COOH (dư) = ( 0.6 - 0.175) * 60 = 25.5 (g)
nCH3COOC2H5 = nC2H5OH = 0.175 (mol)
H% = 0.14/0.175 * 100% = 80%

a)
$C_2H_5OH + CH_3COOH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O$
b)
n CH3COOC2H5 = n C2H5OH = 9,2/46 = 0,2(mol)
=> m este = 0,2.88 = 17,6 gam
c)
n este = 8,8/88 = 0,1(mol)
=> n C2H5OH = n CH3COOH = 0,1/60% = 1/6 mol
=> m C2H5OH = 46 . 1/6 = 7,67(gam) ; m CH3COOH = 60 . 1/6 = 10(gam)
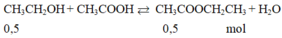
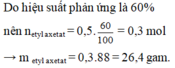

H =50 %
H =50 %