Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Ta có: ![]()
suy ra số mol CO2 trong Z là 0,05 mol tức O bị khử 0,05 mol.
Gọi số mol Fe3O4 và CuO lần lượt là a, b
![]()
Cho Y tác dụng với 1,2 mol HNO3 thu được khí 0,175 mol khí NO2.
Bảo toàn N:
![]()
![]()
Ta có 2 TH xảy ra:
TH1: HNO3 dư.
![]()
![]()
TH2: HNO3 hết.
![]() nghiệm âm loại.
nghiệm âm loại.

2 ancol đơn chức chứ bạn đáp án toàn ancol đơn chức =))
nCO2=0,4 mol nH2O=0,4 mol=>nCO2=nH2O
=>hh gồm các ete no đơn chức
Gọi CTTQ ete là CnH2nO
Bảo toàn klg=>mO2=0,4.44+7,2-7,2=17,6g=>nO2=0,55 mol
Bảo toàn O=>nete=nO trg ete=0,4.2+0,4-0,55.2=0,1 mol
=>Mete=72 g/mol
=>CTPT ete là C4H8O
Chỉ có 1 ctct tm CH2=CH-CH2-O-CH3
=>ete này đc tạo bởi 2 ancol CH3OH và CH2=CH-CH2OH
=>chọn D
Ete + O2 \(\rightarrow\)CO2 + Hoh
số mol ete là x
nCO2 = nhoh = 0.4 \(\rightarrow\) m = \(0,4.\left(18+44\right)=24,8\)
Dựa vào bảo toàn khối lượng: mO2 = 24,8 -7.2 = 17,6\(\rightarrow\) nO2 = 0,55
Bảo toàn nguyên tố oxi: x + 0,55 .2 = 0,4.3\(\rightarrow\) x = 0.1
Mete = 7,2/ 0.1 =72\(\rightarrow\) CH3 - O - C3H5
Đáp án D

Ở 100°C là nhiệt độ cao bắt buộc ra KClO3
nCl2=0,6 mol
nKCl=0,5 mol
3Cl2 +6KOH =>5KCl + KClO3 +3H2O
0,6 mol
0,3 mol <=0,6 mol 0,5 mol
Dư 0,3 mol
CM dd KOH=0,6/2,5=0,24M
=>Chon A!!!!

Đáp án B
Zn có tính khử mạnh hơn Fe, Zn sẽ phản ứng với dung dịch CuSO4 trước.
Theo đề: hỗn hợp rắn Z phản ứng với dung dịch H2SO4 loãng thu được 1 muối duy nhất → trong hỗn hợp rắn Z có Cu và Fe dư. Vậy mFe dư = 0,28 (g) và mCu = 2,84 - 0,28 = 2,56 (g)
Ta có: khối lượng hỗn hợp X phản ứng với Cu2+ = 2,7 - 0,28 = 2,42 (g)
Gọi nZn = x mol; nFe pư = y mol
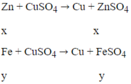
Ta có hệ:
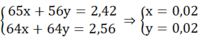
mFe ban đầu = 0,02.56 + 0,28 = 1,4 (g)
![]()

Có 0,1 mol chất béo \(\Rightarrow\) tạo ra 0,1 mol glixerol.
\(\Rightarrow\) m = 0,1 x 92 = 9,2 gam.

Căn cứ vào các tính chất của các halogen ta thấy chỉ có C3H7Cl phản ứng được với dung dịch NaOH đun nóng. Đặt công thức của Y là RCl, phương trình phản ứng :
C3H7Cl + NaOH = C3H7OH + NaCl (1)
mol: x x
AgNO3 + NaCl = AgCl + NaNO3 (2)
mol: x x
Theo (1), (2) và giả thiết ta có :
nC3H7Cl = nNaCl = nAgCl = 1,435/143,5 = 0.01 mol;
mC6H5Cl = 1,91 - 0,01.78,5 = 1,125 gam.

Câu 6:
a) Gọi công thức của X là CxHyOz
Ta có: mC = (13,44 . 12)/22,4 = 7,2 (gam); mH = 9.2/18 = 1 (gam)
MO = 16,2 – 7,2 = 8 (gam)
=>x : y : z = 7,2/12 : 1/1 : 8/16 = 0,6 : 1 : 0,5 = 6 : 10 : 5
Vậy CTPT của X là (C6H10O5), X là polisaccarit.
b) (C6H10O5)n+ nH2O→H+ nC6H12O6.
1 mol n mol
16,2/162n mol a mol
=>a = 0,1 mol
C5H11O5CH=O + 2AgNO3 + 3NH3 + H2O → C5H11O5COONH4 + 2Ag ↓ + 2NH4NO3.
Theo phương trình, ta có: nAg = 0,2 mol
Vì hiệu suất phản ứng bằng 80% =>mAg = (0,2 . 108.80)/100 = 17,28 (gam)

H2=0.6 => h2so4 dư. => trong Y có 0.2 mol H2SO4.
Gọi nAl=a, nFeSO4=b. Ta có: 3a+2b=1.2 và 27a+56b=22.2
=>a=0.2, b=0.3
Dd y: fe2+: 0.3, al3+: 0.2, so4 2-: 0.8 và h- 0.4
Y td vs ba(oh)2 dư
=> kt thu đc là fe(oh)2: 0.3 mol bà baso4 0.8 mol
*lưu ý al3+ k tạo kt vì oh- dư
=> m kt=213.4g
H2=0.6 => h2so4 dư. => trong Y có 0.2 mol H2SO4.
Gọi nAl=a, nFeSO4=b. Ta có: 3a+2b=1.2 và 27a+56b=22.2
=>a=0.2, b=0.3
Dd y: fe2+: 0.3, al3+: 0.2, so4 2-: 0.8 và h- 0.4
Y td vs ba(oh)2 dư
=> kt thu đc là fe(oh)2: 0.3 mol bà baso4 0.8 mol
*lưu ý al3+ k tạo kt vì oh- dư
=> m kt=213.4g
Đáp án D