Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử trong 6,72 lít A có x mol C n H 2 n + 2 y mol C m H 2 m - 2 .
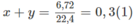
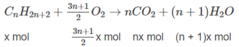
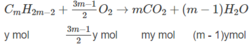
Số mol O 2 :
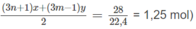
⇒(3n + 1)x + (3m − 1)y = 2,5 (2)
Số mol C O 2 : nx + my = 0,8 (mol)
⇒ (3n + 1)x + (3m - 1)y = 2,5 (3)
Từ (2) và (3) tìm được x - y = 0,1 ;
Kết hợp với X + y = 0,3, ta có: x = 0,2 và y = 0,1 Thay các giá trị tìm được vào (3) ta có
0,2n + 0,1m = 0,8
⇒ 2n + m = 8.
Nếu n = 1 thì m = 6: Loại, vì C 6 H 10 không phải là chất khí ở đktc. Nếu n = 2 thì m = 4. Công thức hai chất là C 2 H 6 và C 4 H 6 .
Nếu n = 3 thì m = 2: Loại vì m > 3.
Trả lời: Hỗn hợp A chứa (66,67%) và C 4 H 6 (33,33%)
Số mol H 2 O = (n + 1)x + (m - 1)y = 0,9 (mol).
2. Khối lượng nước: p = 0,9.18 = 16,2 (g).

Đặt lượng C x H y là a mol, lượng C x + 1 H y + 2 là b mol.
Ta có : a + b = 0,05 (1)
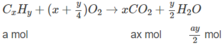
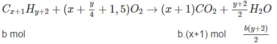
Số mol C O 2 : ax + b(x + 1) = 0,170 (2)
Số mol
H
2
O
: 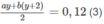
Từ (2) ta có (a + b)x + b = 0,170 ;
b = 0,170 - 0,0500x
b là số mol của một trong hai chất nên 0 < b < 0,0500.
Do đó 0 < 0,170 - 0,0500x < 0,0500 ⇒ 2,40 < x < 3,40 ⇒ x
= 3.
⇒ b = 0,1700 - 0,0500.3 = 0,0200 ⇒ a = 0,0500 - 0,0200 =


Khối lượng bình 2 tăng = mCO2 = 35,2 gam
=> nCO2 = \(\dfrac{35,2}{44}\) = 0,8 mol , nO2 = \(\dfrac{28}{22,4}\) = 1,25 mol
A + O2 → CO2 + H2O
Áp dụng định luật BTNT O => 2nO2 = 2nCO2 + nH2O
=> nH2O = 1,25.2 - 0,8.2 = 0,9 mol
Ankan có CTPT CnH2n+2: x mol
Ankađien có CTPT CmH2m-2 : y mol
CnH2n+2 + O2 → nCO2 + (n+1)H2O
x x.n x.(n+1)
CmH2m-2 + O2 → mCO2 + (m-1)H2O
y y.m y(m-1)
Ta có nH2O - nCO2 = y(m-1) + x.(n+1) - x.n - y.m = x - y = 0,1 (1)
Mà x + y = 0,3 (2)
Từ (1), (2) => x = 0,2 và y = 0,1
%V Ankađien = \(\dfrac{0,1}{0,3}.100\%\)= 33,34%

Số mol các chất trong A là: 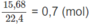
Khi A qua chất xúc tác Ni :
Hỗn hợp B chứa 3 chất: ankan ban đầu
C
n
H
2
n
+
2
, ankan mới tạo ra
C
m
H
2
m
+
2
và anken còn dư
C
m
H
2
m
với số mol tổng cộng là : 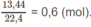
Số mol H 2 trong A là: 0,7 - 0,6 = 0,1(mol).
Khi B qua nước brom thì anken bị giữ lại hết:
C m H 2 m + B r 2 → C m H 2 m B r 2
Hỗn hợp C chỉ còn
C
n
H
2
n
+
2
và
C
m
H
2
m
+
2
với tổng số moi là 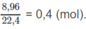
Như vậy, 0,2 mol C m H 2 m có khối lượng 5,6 g, do đó 1 mol C m H 2 m có khối lượng 28 (g) ⇒ m = 2.

Số mol khí trong hỗn hợp A là 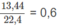
trong B là 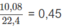
và trong C là 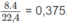
A chứa H 2 , C n H 2 n + 2 và C m H 2 m . Khi A đi qua chất xúc tác
Ni:
C m H 2 m + H 2 → C m H 2 m + 2
B chứa C n H 2 n + 2 , C m H 2 m + 2 và C m H 2 ra còn dư.
Số mol H 2 trong A là: 0,6 - 0,45 = 0,15 (mol).
Đó cũng là số mol C m H 2 m + 2 trong B.
Khi B đi qua nước brom thì C m H 2 m bị giữ lại:
C m H 2 m + B r 2 → C m H 2 m B r 2 .
Số mol C m H 2 m trong B là: 0,45 - 0,375 = 0,075 (mol).
Khối lương 1 mol
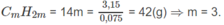
Anken là C 3 H 6 và ankan do chất đó tạo ra là C3H8.
Trong hỗn hợp c có 0,15 mol C 3 H 8 và 0,375 - 0,15 = 0,225 mol C n H 2 n + 2
Khối lượng hỗn hợp C là: 0,375. 17,8. 2 = 13,35 (g).
⇒ 0,15.44 + 0,225(14n + 2) = 13,35
⇒ n = 2 Ankan là C 2 H 6 .
A chứa C 2 H 6 (37,5%); C 3 H 6 (37,5%) và H2 (25%) ;
B chứa C 2 H 6 (50%); C 3 H 8 (33,3%) và C 3 H 6 (16,7%); C chứa C 2 H 6 (60%) và C 3 H 8 (40%).

Gọi công thức phân tử của X là CxHyOz .
Sản phẩm cháy gồm CO2 và H2O.
Ở lần thí nghiệm thứ nhất, bình 1 chứa H2SO4 đậm đặc dư hấp thụ H2O và bình 2 chứa dung dịch nước vôi trong dư hấp thụ CO2.
Ở lần thí nghiệm thứ hai, bình 1 chứa CaO dư hấp thụ CO2 và toàn bộ hơi nước, bình 2 chứa P2O5 dư không hấp thụ gì vì toàn bộ lượng khí đã được hấp thụ ở bình 1. Do đó m2 = 0. Theo định luật bảo toàn khối lượng ta có
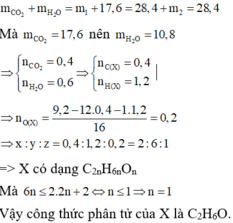

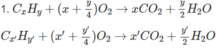
H 2 S O 4 + n H 2 O → H 2 S O 4 .n H 2 O
2NaOH + C O 2 → N a 2 C O 3 + H 2 O
Số mol
C
O
2
là: 
Khối lượng C trong hỗn hợp A là: 0,095.12 = 1,14 (g).
Khối lượng H trong hỗn hợp A là: 1,3 - 1,14 = 0,16 (g).
Số mol
H
2
O
sau phản ứng là: 
Để tạo ra 0,095 mol C O 2 cần 0,095 mol O 2 ;
Để tạo ra 0,08 mol H 2 O cần 0,04 (mol) O 2 .
Số mol O 2 đã tham gia phản ứng là: 0,095 + 0,04 = 0,135 (mol).
Số mol
O
2
ban đầu là: 
Số mol O 2 còn dư là: 0,155 - 0,135 = 0,02 (mol).
Số mol 3 chất trong bình sau phản ứng:
0,095 + 0,08 + 0,02 = 0,195 (mol).
Nếu ở đktc thì V O = 0,195.22,4 = 4,37 (lít).
Thực tế V2 = 8,4 lít
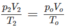
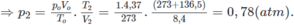
2. Đổi thể tích hỗn hợp khí trước phản ứng về đktc:
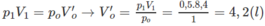
Số mol khí trước phản ứng: 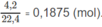
Số mol 2 hiđrocacbon: 0,1875 - 0,155 = 0,0325 (mol).
Đặt lượng C n H 2 n là a mol, lượng C m H 2 m - 2 là b mol, ta có a + b = 0,0325.
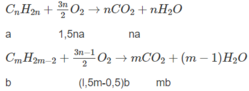
Số mol O 2 : l,5na + (l,5m - 0,5)b = 0,135 (2)
Số mol C O 2 : na + mb = 0,095 (3)
Từ (2) và (3), tìm được b = 0,015 ⇒ a = 0,0175
Thay các giá trị của a và b vào (3), ta có :
1,75. 10 - 2 n + 1,5. 10 - 2 m = 9,5. 10 - 2
7n + 6m = 38
Nếu n = 2 thì 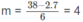
Nếu n = 3 thì 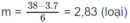
Nếu n > 3 thì m < 2 (loại).
% về thể tích của
C
2
H
4
: 
% về thể tích của C 4 H 6 là 46,2%

