Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình ion rút gọn :
a) Ca2+ + CO32- → CaCO3 ↓
b) Fe2+ + 2OH- → Fe(OH)2↓
c) HCO3- + H+ → CO2 ↑ + H2O
d) HCO3- + OH- → H2O + CO32-
e) Không có phương trình ion rút gọn.
g) Pb(OH)2(r) + 2H+ → Pb2+ + 2H2O
h) H2PbO2(r) + 2OH- → PbO22- + 2H2O
i) Cu2+ + S2- → CuS↓.

Phương trình phân tứ và ion xảy ra trong dung dịch :
a) Fe2(SO4)3 + 6NaOH → 2Fe(OH)3\(\downarrow\) + 3Na2SO4
2Fe3+ + 3SO42- + 6Na+ + 6OH- → 2Fe(OH)3\(\downarrow\)+ 6Na+ + 3SO42-
Fe3+ + 3OH- → Fe(OH)3\(\downarrow\)
b) NH4Cl + AgNO3 → NH4NO3 + AgCl↓
NH4 + Cl- + Ag+ + NO3- → NH4+ + NO3- + AgCl↓
Cl- + Ag+ → AgCl↓
c) NaF + HCl → NaCl + HF↑
Na+ + F- + H+ + Cl- → Na+ + Cl- + HF↑
F- + H+ → HF\(\uparrow\)
d) Không có phản ứng xảy ra
e) FeS(r) + 2HCl → FeCl2 + H2S ↑
FeS(r) + 2H+ + 2Cl- → Fe2+ + 2Cl- + H2S↑
FeS(r) + 2H+ \(\rightarrow\) Fe2+ + H2S↑
g) HClO + KOH \(\rightarrow\) KClO + H2O
HClO + K+ + OH- \(\rightarrow\) K+ + CIO- + H2O
HClO + OH- \(\rightarrow\) CIO- + H2O.

1,
CaC2 + 2H2O → C2H2 + Ca(OH)2
3C2H2 → C6H6
C6H6 + 3Cl2 → C6H6Cl6
2,
C6H6 + Br2 → C2H5Br + HBr
3,
C6H6 + CH3Cl → C6H5CH3 + HCl
C6H5CH3 + 3HNO3 → 3H2O + C6H2CH3(NO3)2
4,
C6H6 + C2H5Cl → HCl + C6H5CH2CH3
C6H5CH2CH3 → H2 + C6H5CHCH2
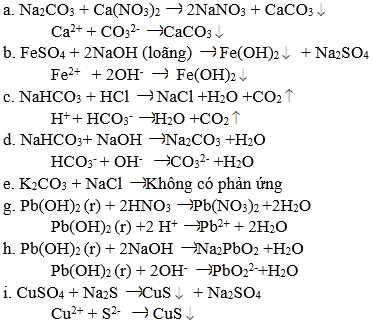
Đáp án B
Đặt CTTQ của ankan A là CnH2n+2.
Phương trình phản ứng:
400ml 800ml
Ta có tỉ lệ: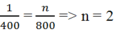
Vậy CTPT của A là C2H6.