Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CH4 -> CO2
C2H6 -> 2 CO2
Gọi nCH4 = x mol, nC2H6 = y mol
x + y = 0,15 (1)
x + 2y = 0,2 (2)
Nên: x = 0,1 mol, y = 0,05 mol
Vậy: % VCH4 = 66,67 % => %VC2H6 = 33,33 %

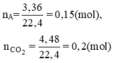
Gọi số mol của metan và etan lần lượt là x và y (mol)
Phương trình phản ứng:
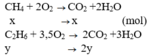
Vậy thành phần phần trăm về thể tích các khí trong hỗn hợp A là:
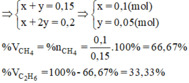

- Gọi mol metan và etan là x, y ( mol )
\(x+y=n_{hh}=\dfrac{V}{22,4}=0,25\left(mol\right)\)
Lại có : \(x+2y=n_{CO_2}=\dfrac{V}{22,4}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\) ( mol )
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_4}=1,6\left(g\right)\\m_{C_2H_6}=4,5\left(g\right)\end{matrix}\right.\)
=> mhh = 6,1 ( g )
=> %mCH4 = ~ 26,22%
=> %mC2H6 = ~73,78%
Ta có : \(\%V_{CH4}=\dfrac{V}{Vhh}=40\%\)
=> %VC2H6 = 100 - %VCH4 = 60% .
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_6+5O_2\underrightarrow{t^o}4CO_2+6H_2O\)
Giả sử: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_6}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{5,6}{22,4}=0,25\left(1\right)\)
Ta có: \(n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(\Sigma n_{CO_2}=n_{CH_4}+2n_{C_2H_6}\)
\(\Rightarrow x+2y=0,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,25}.100\%=40\%\\\%V_{C_2H_6}=60\%\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,1.16}{0,1.16+0,15.30}.100\%\approx26,2\%\\\%m_{C_2H_6}\approx73,8\%\end{matrix}\right.\)
Bạn tham khảo nhé!

Chất khí bay ra chính là metan ⇒ nCH4 = nCO2 = 5,544 : 44 = 0,126 mol
VCH4 = 0,126.22,4 = 2,8224 lít
⇒ %VCH4 = (2,8224 : 10,8 ).100% = 26,13%
⇒ %Volefin = 73,87%
Đáp án A

Đáp án A
hhX gồm CH4 và CnH2n
10,8 lít hhX + Br2 thấy có CH4 bay ra.
CH4 + O2 → 0,126 mol CO2
→ nCH4 = 0,126 x 22,4 = 2,8224 lít →
%
V
C
H
4
=
2
,
8224
10
,
8
≈
26
,
13
%
; %VCnH2n ≈ 73,87%

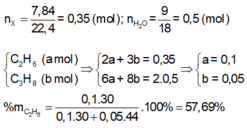
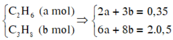
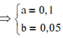
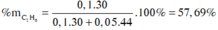
\(n_{CH_4} = a\ mol ;n_{C_2H_6} = b\ mol\\ \Rightarrow a + b = \dfrac{3,36}{22,4}= 0,15(1)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_6 + \dfrac{7}{2}O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O\\ n_{CO_2} = a + 2b = \dfrac{4,48}{22,4} = 0,2(2)\\ (1)(2) \Rightarrow a = 0,1 ;b = 0,05\\ \Rightarrow \%V_{CH_4} = \dfrac{0,1}{0,15}.100\% = 66,67\%\\ \%V_{C_2H_6} = 100\% - 66,67\% = 33,33\%\)
\(n_{CH_4}=a\left(mol\right),n_{C_2H_6}=b\left(mol\right)\)
\(\Rightarrow a+b=0.15\left(mol\right)\left(1\right)\)
\(n_{CO_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(\Rightarrow a+2b=0.2\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
\(\%CH_4=\dfrac{0.1}{0.15}\cdot100\%=66.67\%\)
\(\%C_2H_6=33.33\%\)